吡啶(Pyridine),又名氮苯,是含有一个氮杂原子的六元杂环化合物,无色或微黄色液体,有恶臭。在工业上除作为溶剂以外,还可用作变性剂、助染剂,以及合成一系列产品(包括药品、消毒剂、染料、食品调味料、黏合剂、炸药等)的起始物,也可以对金属起到缓蚀作用,属于2B类致癌物,长期接触可能导致人体神经系统和心血管系统的病变和损伤[1-2]。
目前,吡啶的常用检测方法有分光光度法[3-4]、气相色谱法[5-10]、气相色谱-质谱法[11-12]、液相色谱-质谱法[13]等。其中,分光光度法干扰较大,气相色谱-质谱法和液相色谱-质谱法的检测仪器价格相对较高,而气相色谱法的应用最为普遍。《工作场所空气有毒物质测定杂环化合物》(GBZ/T 160.75—2004)中[14],采用的方法是用碱性活性炭采样管采集,二氯甲烷解吸,气相色谱FID检测器分析空气中吡啶,但在实际分析过程中发现,该方法空白加标回收率偏低,测定结果难以反映吡啶的实际浓度水平。现优化了样品采集、样品前处理和气相色谱参数,改用GDX 502采样管采样,二氯甲烷解吸,气相色谱法测定气中的吡啶。
1 实验部分 1.1 仪器和试剂 1.1.1 仪器7890A型气相色谱仪(美国Agilent公司),配备氢火焰离子化检测器(FID);DB-1色谱柱(30 m×250 μm×0.25 μm,美国Agilent公司);KB-6E型大气采样器(青岛金仕达电子科技有限公司);GH-1型活性炭采样管(6 mm×80 mm,填料100/50 mg,南通金南玻仪五金厂);GH-1型碱性活性炭采样管(6 mm×80 mm,填料100/50 mg,南通金南玻仪五金厂);GDX 502采样管(200 mg,南通金南玻仪五金厂)。
1.1.2 试剂CNW二硫化碳(低苯级,上海安谱试验科技股份有限公司);二氯甲烷(色谱纯,美国SIGMA-ALORICH公司);甲醇(农残级,美国J.T.Baker公司);丙酮(色谱纯,德国Merck公司);正己烷(色谱纯,美国TEDIA公司);乙酸乙酯(色谱纯,德国Merck公司);吡啶(99.5%,德国Dr.Ehrenstorfer公司)。载气:高纯氮气(纯度≥99.999 %,南京天泽气体有限责任公司)。
1.2 实验操作 1.2.1 样品采集与保存活性炭采样管和碱性活性炭采样管须敲开两端,将入气口与采样器相连,GDX 502采样管的入气口可直接与采样器相连,须检查系统的气密性。若现场大气中含有较多颗粒物,可在采样管前连接过滤头采集样品。采样时记录采样器流量、当前温度、气压及采样时间和地点。采样完毕后,取下采样管,立即用聚四氟乙烯帽密封,常温下避光保存。
1.2.2 气相色谱条件进样方式:分流进样,分流比10:1,进样体积1.0 μL;进样口温度270 ℃,检测器温度280 ℃;色谱柱升温程序:起始柱温40 ℃,以15 ℃/min升至115 ℃,再以30 ℃/min升至260 ℃;气体流量:柱流量1.0 mL/min,氢气35 mL/min,空气300 mL/min,尾吹气30 mL/min。
1.2.3 样品预处理活性炭采样管、碱性活性炭采样管:将活性炭采样管或碱性活性炭采样管中的活性炭取出,放入磨口具塞试管中,向试管中加入1.00 mL解吸液,轻轻振动,在室温下解吸30 min,解吸液转移至进样小瓶中,待测。
GDX 502采样管:将采样管进气端竖直向上固定,下端接进样小瓶,用滴管从采样管上端滴加解吸溶剂进行解吸,溶剂不可溢出采样管顶端,接收解吸液1.0 mL,待测。
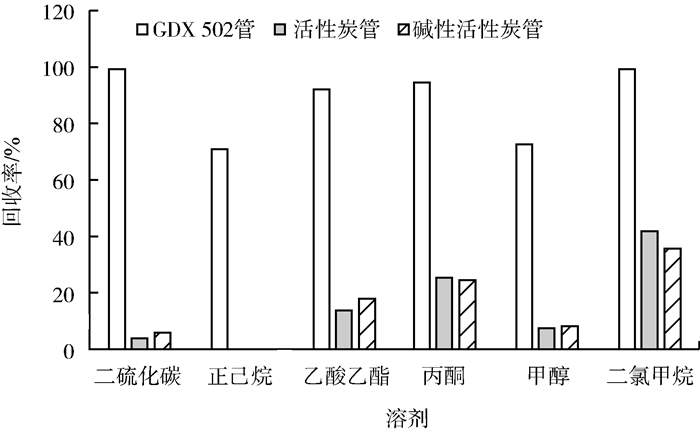
2 结果与讨论 2.1 采样管和解吸溶剂的选择分别选用了活性炭管和GDX 502管,并与标准方法《GBZ/T 160.75—2004》中规定的碱性活性炭管作比较,在吡啶加入量为19.6 μg时,考察了用二硫化碳、正己烷、乙酸乙酯、丙酮、甲醇、二氯甲烷这6种不同极性溶剂为解吸液时吡啶的解吸效率,见图 1。
|
| 图 1 不同溶剂对采样管中吡啶解吸效率的影响 |
由图 1可见,6种溶剂对活性炭管中吡啶和碱性活性炭管中吡啶的解吸效率接近,总体较低,其中正己烷无法解吸采样管中的吡啶,二氯甲烷的解吸效率最高,但也仅在40%左右,均无法满足分析要求。
6种溶剂对GDX 502管中吡啶的解吸效率均高于上述2种采样管,采用正己烷或甲醇解吸时,解吸效率相对偏低,在70%左右,采用二硫化碳、乙酸乙酯、丙酮和二氯甲烷解吸时,解吸效率均>90%。由于乙酸乙酯中含有较多杂质,会干扰吡啶的测定;丙酮为易制毒试剂,采购程序较烦琐;二硫化碳毒性较高。因此最终确定用GDX 502管吸附,用二氯甲烷解吸。
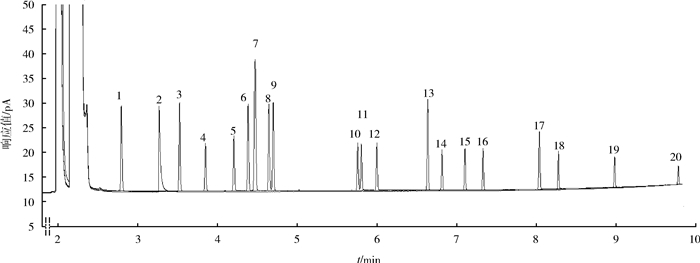
2.2 干扰及消除GDX 502管是《大气固定污染源氯苯类化合物的测定气相色谱法》(HJ/T 66—2001)[15]中规定的采集氯苯类污染物的采样管,苯系物、乙酸丁酯、正十一烷等挥发性有机物是环境空气和废气中常见的污染物,因此,考察了上述物质对吡啶测定的干扰,在上述选定的色谱条件下,苯系物、乙酸丁酯、正十一烷和氯苯类等21种物质均不干扰吡啶的测定,吡啶与21种物质的气相色谱图见图 2。
|
| 1—苯; 2—吡啶; 3—甲苯; 4—乙酸丁酯; 5—氯苯; 6—乙苯; 7—对/间二甲苯; 8—苯乙烯; 9—邻二甲苯; 10—1, 4-二氯苯; 11.1, 3-二氯苯; 12—1, 2-二氯苯; 13—正十一烷; 14—1, 3, 5-三氯苯; 15—1, 2, 4-三氯苯; 16—1, 2, 3-三氯苯; 17—1, 2, 3, 5-四氯苯/1, 2, 4, 5-四氯苯; 18—1, 2, 3, 4-四氯苯; 19—五氯苯; 20—六氯苯。 图 2 吡啶与21种物质的气相色谱图 |
2.3 采样时间、流量对富集效率的影响
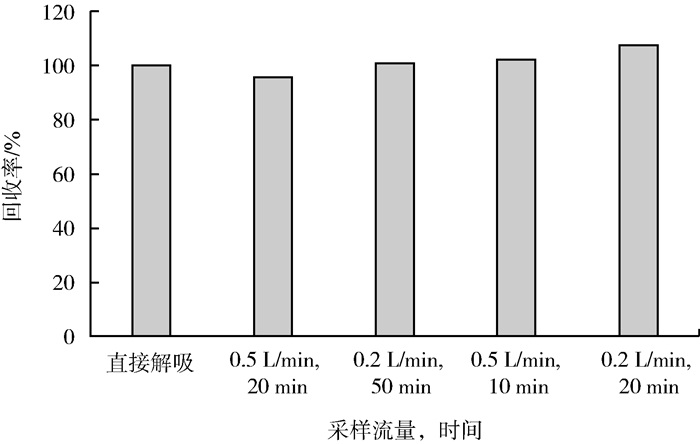
在GDX 502采样管中加入一定量的吡啶标准溶液,并将采样管连接在大气采样器上,调节采样时间和采样流量,模拟实际采样过程,采集一定体积的不含吡啶的空气,以二氯甲烷解吸样品,考察采样时间10,20和50 min以及流量0.2和0.5 L/min时对样品的富集效率的影响,见图 3。
|
| 图 3 采样流量和时间对富集效率的影响 |
由图 3可见,采样时间为10~50 min、流量≤0.5 L/min,吡啶在GDX 502管中的回收率为90%~110%,采样时间和采样体积对富集效率的影响不大。由于0.5 L/min是常用的采样流量,采样时间过短会影响方法的灵敏度,综合考虑,确定以0.5 L/min的流量采集样品20 min,采样体积为10 L。
2.4 穿透实验和解吸溶剂体积的选择串联2支含200 mg GDX 502的采样管,1#采样管中加入一定体积的吡啶标准溶液,吡啶的加标量分别为391和489 μg,以0.5 L/min的流量采集20 min不含吡啶的空气,采样完成后,1#采样管每次用二氯甲烷洗脱至1 mL,共洗脱4次,2#采样管每次用二氯甲烷洗脱至1 mL,共洗脱3次,所有洗脱液均单独收集并分别测定,考察解吸溶剂体积对解吸效率的影响和采样管的吸附容量,见表 1。
| 吡啶加标量/μg | 1#采样管洗脱次数 | 2#采样管洗脱次数 | 2支采样管总回收率/% | 2#与1#采样管量比值/% | |||||||
| 1 | 2 | 3 | 4 | 1 | 2 | 3 | |||||
| 391 | 测定值/μg | 369 | 0.83 | — | — | — | — | — | 94.6 | 0 | |
| 回收率/% | 94.4 | 0.2 | 0 | 0 | 0 | 0 | 0 | ||||
| 489 | 测定值/μg | 339 | 2.72 | — | — | 95.8 | 4.39 | — | 90.4 | 29.3 | |
| 回收率/% | 69.3 | 0.56 | 0 | 0 | 19.6 | 0.90 | 0 | ||||
| ①—为未检出。 | |||||||||||
由表 1可见,当加标量为391 μg、二氯甲烷解吸时,1#采样管解吸至1 mL的回收率为94.4%,2#采样管未检出吡啶,表明1 mL二氯甲烷能完全解吸<391 μg的吡啶;当加标量增加到489 μg时,2#采样管量与1#采样管量比值达29.3%,表明采样管已经穿透,因此确定200 mg GDX 502管的最大吸附量为391 μg,采用二氯甲烷解吸,解吸体积1 mL。
2.5 线性范围和检出限用微量注射器准确移取10.0 μL的吡啶至盛有适量二氯甲烷的10 mL容量瓶中,定容至刻度线,配制成质量浓度为978 mg/L的标准储备液,再分别准确移取5.0,10.0,25.0,50.0和100.0 μL的标准储备液至盛有适量二氯甲烷的5 mL容量瓶中,定容至刻度线,配制成系列标准溶液,并在选定的条件下进行测试。方法的线性回归方程为y=1.31 x-0.27,相关系数为0.999 9。
由于空白的GDX 502采样管中未检出吡啶,所以以选定仪器条件下色谱响应2~3倍信噪比对应的吡啶含量为预估检出限,向GDX 502采样管内注入0.489 μg的吡啶标准溶液,按照实际样品的分析步骤平行测定7次,按公式MDL=3.143×S(S为7次测定结果的标准偏差)计算方法的检出限为0.1 μg。当采样体积为10 L时,方法检出限为0.01 mg/m3,<0.3 mg/m3(以采集1.5 L空气样品计, 《GBZ/T 160.75—2004》中的检出限标准)。
2.6 精密度和准确度向空白的GDX 502采样管中分别加入1.96,9.78和19.6 μg的吡啶标准溶液,平行测定6次,相对标准偏差(RSD)为2.9%~4.4%,加标回收率为90.8%~108%,见表 2。
| 本底值/μg | 加标量/μg | 测定均值/μg | RSD/% | 加标回收率/% |
| — | 1.96 | 2.04 | 3.6 | 98.5~108 |
| — | 9.78 | 9.54 | 2.9 | 93.8~101 |
| — | 19.6 | 19.0 | 4.4 | 90.8~104 |
| ①—为未检出。 | ||||
2.7 实际样品的测定
用该方法对某厂界空气和车间空气样品进行测定,结果见表 3。
3 结语
优选GDX 502管采集,二氯甲烷解吸至1 mL,气相色谱分离检测的方法测定气中吡啶。该方法富集效率高,抗干扰能力强,操作简单,线性良好,方法检出限、精密度和回收率均可以满足气中吡啶的监测要求。
| [1] |
陈民孝. 急性吡啶中毒25年临床追踪观察(附1例典型病例)[J]. 中国工业医学杂志, 1989, 2(2): 28-29. |
| [2] |
顾林生, 马新华, 邢岩, 等. 慢性吡啶中毒1例报告[J]. 职业与健康, 1997, 13(2): 37-38. |
| [3] |
杨梅桂, 王窕人. 用泡腾片做氧化剂的分光光度法测定空气中吡啶的探讨[J]. 职业与健康, 2007, 23(8): 606-607. DOI:10.3969/j.issn.1004-1257.2007.08.018 |
| [4] |
《空气和废气监测分析方法》编委会. 空气和废气监测分析方法[M]. 4版增补版. 北京: 中国环境科学出版社, 2003: 707-709.
|
| [5] |
王艳丽, 周阳, 李利荣. 顶空进样-气相色谱法测定大气中吡啶的研究[J]. 中国环境监测, 2013, 29(2): 62-64. DOI:10.3969/j.issn.1002-6002.2013.02.013 |
| [6] |
刘玉斌. 顶空-气相色谱法测定卷烟主流烟气粒相物中吡啶[J]. 中国测试, 2014, 40(2): 61-63. |
| [7] |
朱琳, 姜红梅, 杨丽君. 居住区大气中吡啶的溶剂解吸毛细管气相色谱测定法[J]. 环境与健康, 2011, 28(6): 540-541. |
| [8] |
徐秋军, 鲁宝权, 龚晓丽, 等. 空气和废气中吡啶检测分析方法研究[J]. 环境科学导刊, 2012, 31(6): 113-114. DOI:10.3969/j.issn.1673-9655.2012.06.031 |
| [9] |
夏荣波. 毛细管柱气相色谱法同时测定大气中的四氢呋喃和吡啶[J]. 污染防治技术, 2012, 25(6): 59-61. |
| [10] |
马莉. 气相色谱法测定环境空气中吡啶[J]. 北方环境, 2013, 25(6): 166-167. DOI:10.3969/j.issn.1007-0370.2013.06.051 |
| [11] |
吉正元, 普学伟. 吹扫捕集-气相色谱/质谱法测定水中的乙醛、丙烯醛、丙烯腈、吡啶、松节油和丁基黄原酸[J]. 环境监控与预警, 2017, 9(5): 16-19. DOI:10.3969/j.issn.1674-6732.2017.05.005 |
| [12] |
张文锦. 气相色谱-质谱法测定水中四氢呋喃和吡啶的含量[J]. 理化检验(化学分册), 2017, 53(7): 821-823. |
| [13] |
刘建明, 樊杰, 赵瑞花, 等. 液相色谱-质谱联用测定卷烟主流烟气中的吡啶等氮杂芳烃[J]. 分析试验室, 2017, 36(11): 1302-1305. |
| [14] |
中华人民共和国卫生部.工作场所空气有毒物质测定杂环化合物: GBZ/T 160.75—2004[S].北京: 人民卫生出版社, 2004.
|
| [15] |
国家环境保护总局.大气固定污染源氯苯类化合物的测定气相色谱法: HJ/T 66—2001[S].北京: 中国环境科学出版社, 2001.
|

