2. 国家地表水环境有机污染物监测分析重点实验室,江苏 南京 210019
2. State Environmental Protection Key Laboratory of Monitoring and Analysis for Organic Pollutants in Surface Water, Nanjing, Jiangsu 210019, China
改善空气质量已成为我国最重要的环境保护任务之一,挥发性有机物(VOCs)是造成臭氧(O3)污染的重要前体物, 其大气化学反应的产物也是细颗粒物(PM2.5)中的重要组分,是导致灰霾天气的重要前体物,也是治理空气污染的关键[1-5]。2021年2月,生态环境部指出,VOCs取代二氧化硫(SO2)成为“十四五”城市空气质量考核新指标。精准监测是污染治理的前提和基础,目前用于测定环境空气中VOCs的主要方法为《环境空气挥发性有机物的测定罐采样/气相色谱-质谱法》(HJ 759—2015)和生态环境部发布的《2018年重点地区环境空气挥发性有机物监测方案》(环办监测函〔2017〕2024号),该方法灵敏度高、重现性好,但在监测过程中存在的诸多细节要求和注意事项并没有体现在方法文本中,可能影响监测数据的准确性。现在大量实验室分析经验和对全国多个环境监测中心进行调研的基础上,浅析了罐采样/气相色谱-质谱法测定VOCs在多个环节中的注意事项,以供VOCs监测人员参考。
1 实验部分 1.1 主要仪器与试剂仪器:Agilent 7890A/5977B型气相色谱-质谱仪(美国安捷伦公司);ENTECH 7200型大气浓缩仪、ENTECH 4700型静态稀释仪、ENTECH 3100型苏玛罐清洗仪(美国ENTECH公司);DB-624色谱柱(60 m×0.25 mm×1.4 μm,美国安捷伦公司)。
试剂:VOCs标准储备气(1.00 μmol/mol,中国测试技术研究院),包含丙烯等64种有毒挥发性有机物(TO-15)组分,底气为高纯氮气。
1.2 冷阱浓缩条件一级冷阱捕集温度为-40 ℃,解吸温度为10 ℃;二级冷阱捕集温度为-60 ℃, 解吸温度为220 ℃;三级预热温度为-180 ℃,聚焦温度为-175 ℃。
1.3 仪器分析条件 1.3.1 色谱条件进样口温度:200 ℃;载气:高纯氦气,分流比:15 ∶ 1,恒流1.0 mL/min;升温程序:初始温度5 ℃,保持6 min,以5 ℃ /min升至170 ℃,保持5 min,再以15 ℃/min升至190 ℃。
1.3.2 质谱条件离子源:电子轰击离子源(EI源);溶剂延迟时间: 0.5 min;接口温度: 230 ℃;离子源温度: 230 ℃;四极杆温度:150 ℃;传输线温度:230 ℃;采集方式:全扫描模式(SCAN);扫描范围:35~300 amu。
2 技术要点研究及讨论 2.1 采样前及采样环节技术要点讨论 2.1.1 流量控制器和过滤器的校准检查流量控制器和过滤器分别被用来进行恒流采样和过滤环境空气中的颗粒物。流量控制器的核心部件是限流阀,通过改变其孔径来调节样品采集流量,规格为1~24 h不等,其中24 h的流量控制器孔径最小,在实际采样过程中容易被堵塞。过滤器通过≤10 μm的小孔对空气样品进行过滤,在采样过程中也容易被堵塞。在VOCs监测的实际工作中,时常有采样罐未采集到样品的情况,其可能原因是流量控制器或过滤器堵塞导致。因此应在采样前对流量控制器及过滤器进行流量校准核查,并在采样后及时检查和记录采样罐压力。
2.1.2 采样罐性能检查采样罐性能包括气密性和内壁惰性2个方面,其优劣程度对VOCs样品保存及分析的影响很大。如果气密性不达标,则不利于样品中丙烯等低沸点VOCs组分的保存,容易产生散逸损失;如果内壁惰性不达标,则不利于高沸点或极性组分的保存,容易对这些组分产生吸附作用。但如果每次采样前对采样罐逐个进行性能检查,则工作量巨大,不利于实际操作和推广。因此建议按一定比例抽查,并轮流抽测不同采样罐,确保在一定时间周期内完成对所有采样罐的检查,可大大降低因采样罐漏气或罐内壁惰性不达标而导致样品无效的风险。
2.1.3 样品的采集、运输及保存采样时,要尽量避免外界环境对样品代表性的干扰,应避开有机动车行驶的马路,以及抽烟人群和空调外机等。采样前,要记录采样罐压力,核查罐内是否呈真空状态,压力表上的压力是否在-30 inHg(-101.58 kPa)附近。采样后,要核查采样罐内是否呈微负压状态,罐内气压与环境空气压差是否为-17~-7 kPa,否则应检查采样系统;若压差达到-34~-17 kPa,则应重点检查是否为流量控制器或过滤器堵塞所致;若压差为-7~0 kPa,则应检查是否为采样罐气密性不合格所致。
样品运送过程中,罐口要盖上螺旋盖,避免罐口污染影响罐体的气密性。采样后应尽快分析,保存时间不得超过20 d,否则将增大丙烯等低沸点物质散逸损失的风险。
2.2 实验室分析环节技术要点讨论 2.2.1 色谱柱的选择丙烯等64种VOCs涉及烷烃类、烯烃类、醛酮类、芳香烃类、卤代烃类和卤代芳香烃类等多个化合物种类,沸点范围较大(-50~220 ℃)。因此在色谱柱选择上柱长锁定为60 m,以中等极性色谱柱DB-624(固定液为6%的腈丙基苯基+94%的二甲基聚硅氧烷)、弱极性色谱柱DB-5 ms(固定液为5%的二苯基+95%的二甲基聚硅氧烷)和非极性色谱柱DB-1 ms(固定液为100%的二甲基聚硅氧烷)这3种色谱柱为研究对象,均购自美国安捷伦公司。强极性色谱柱因其不耐高温,柱流失较大而无法有效分析多组分的VOCs,故不在考察之列。
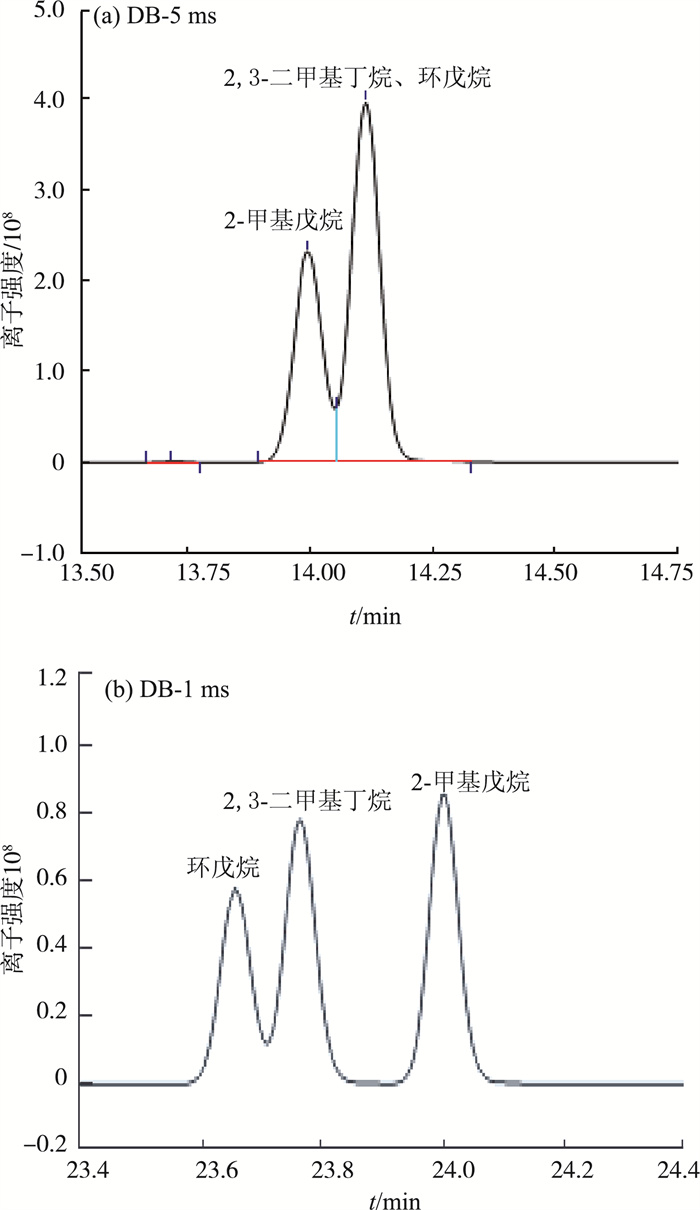
实验结果表明,当气相色谱仪柱温箱有冷阱,柱温起始温度为-20~0 ℃时,DB-1 ms在耐低温方面优于DB-624,在对烷烃类分离上优于DB-5 ms。DB-1 ms和DB-5 ms对2, 3-二甲基丁烷、2-甲基戊烷及环戊烷的分离能力见图 1(a)(b)。由图 1可见,DB-1 ms对2, 3-二甲基丁烷、2-甲基戊烷及环戊烷的分离效果更好,性能更优。
|
图 1 DB-1ms和DB-5ms对2, 3-二甲基丁烷、2-甲基戊烷及环戊烷分离能力比较 |
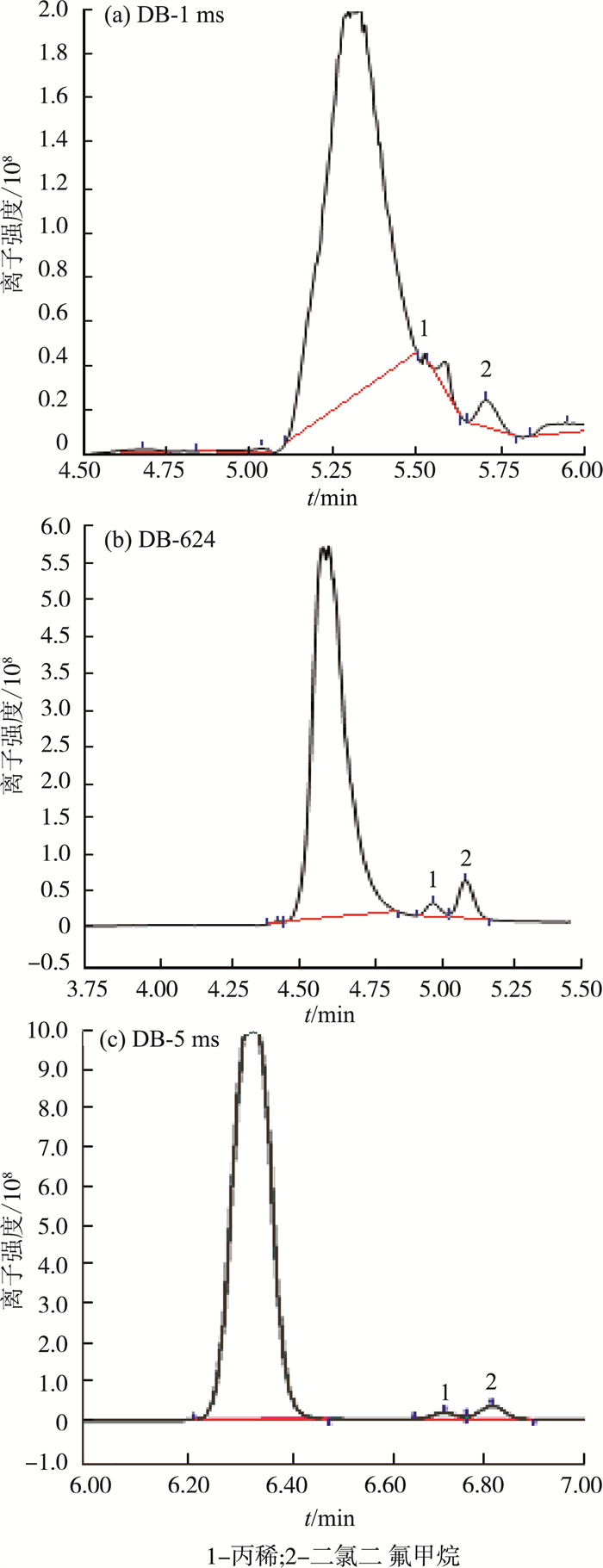
当气相色谱仪柱温箱没有冷阱,柱温起始温度为室温时,由于丙烯和二氯二氟甲烷峰形会受CO2峰的影响,导致这2种物质的灵敏度下降,因此DB-1 ms的分离效果劣于DB-624和DB-5 ms,见图 2(a)(b)。
|
图 2 3种不同色谱柱对丙烯和二氯二氟甲烷分离能力的比较 |
综上所述,在不使用柱温箱冷阱的情况下,推荐使用DB-624和DB-5ms;当采用柱温箱冷阱时,推荐使用DB-1ms。
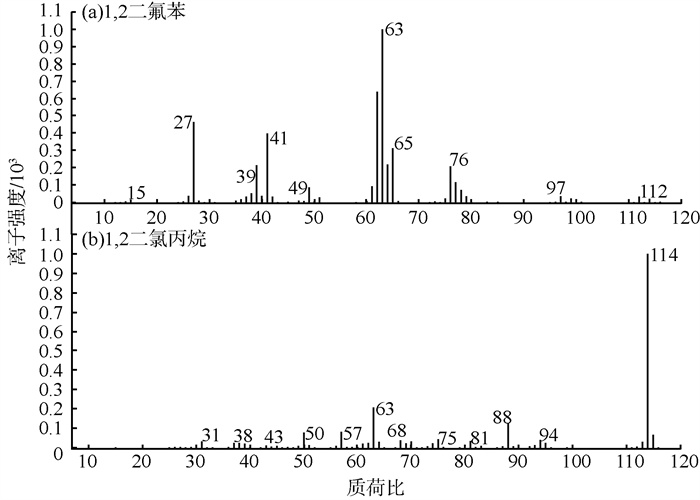
2.2.2 内标物的选择方法标准《HJ 759—2015》中推荐的内标物是一溴一氯甲烷、1, 2-二氟苯、氯苯-d5中的1~3种物质。在实验中发现,当色谱柱为DB-1 ms时,内标物1, 2-二氟苯与目标组分1, 2-二氯丙烷几乎完全重叠(保留时间分别为16.34和16.42 min),且共同具有质荷比为75和63的碎片离子见图 3(a)(b),因而产生正干扰。因此,当采用DB-1 ms时,建议将内标物由1, 2-二氟苯改为1, 4-二氟苯。1, 4-二氟苯的出峰时间较1, 2-二氟苯提前0.5 min,能够实现与1, 2-二氯丙烷的有效分离,从而避免相互间干扰。
|
图 3 1, 2-二氟苯与1, 2-二氯丙烷的质谱图 |
虽然除水是VOCs在分析前处理中的重要环节,但在样品的保存过程中却需要有一定水分存在。熊华竞等[5-8]研究表明,实际样品与气体标准物质基体湿度的差异可能影响色谱行为和最终检测结果的准确性。因为对于极性色谱柱而言,样品中的水分可能影响化合物的色谱峰保留时间,并且水分子可以通过抢占样品罐内壁活点,从而降低罐内壁对VOCs组分尤其是高沸点或强极性组分的吸附,如萘、氯代甲苯和1,4-二噁烷等。实际环境空气样品均带有一定的湿度,而标准气体相对干燥,需要在配制过程中加入一定的水量。经实验验证,加湿后,大部分化合物未发生显著变化,而萘、氯代甲苯和1,4-二噁烷等化合物,在仪器上的响应明显提高,提高了15%~30%,标准曲线的线性明显更优。
2.2.4 气体稀释仪对分析结果的影响用于稀释和配制VOCs标准气体的稀释仪,从其工作原理上可分为静态稀释仪和动态稀释仪。其中采用静态稀释仪稀释时,在配制过程中标准气体没有得到充分混匀,需要放置平衡后使用。否则目标物的浓度响应不稳定,标准曲线的线性关系不佳,容易超出方法规定的质控范围。美国环保局新修订的EPA TO15a-2019方法也对此做出了平衡的要求[9]。
2.2.5 标准曲线绘制方式在《HJ 759—2015》标准中,标准曲线绘制方式是配制1个标准使用气,通过不同取样体积,达到绘制标准曲线的目的。这种方法因降低了标准使用气体的配制数量,更便于操作,而被各个实验室广泛使用。但当标准气体稀释或保存环节出现问题时,因只有1个标准使用气体而问题不容易被发现。因此,建议绘制标准曲线时至少使用2个不同浓度的标准使用气体,推荐浓度为5.0和40.0 nmol/mol。
2.2.6 系统性能优劣的判断对于《HJ 759—2015》标准中65种TO-15组分,检测的难点是高沸点、高活性或极性物质,主要包括萘、1,2,4-三氯苯、氯代甲苯、丙酮、丙烯醛和1,4-二噁烷等,这些目标组分在测定中的灵敏度和曲线方程的线性关系可以用于判断系统性能的优劣。如果所有组分的响应均有所降低,要重点排查是否分析系统受到污染而导致仪器灵敏度下降;如果仅仅是上述几种组分的响应有异常,则要排查样品罐或分析系统是否存在会对这些组分产生吸附作用的活点。
3 结语真空罐/气相色谱-质谱法是我国目前用于环境空气中VOCs监测的主要方法,该方法具有无动力采样、灵敏度高、重现性好等优点,但要在采样前对过滤器、流量控制器和采样罐做性能检查,采样后要记录采样罐压力,及时判断样品采集的有效性。在实验室分析环节要选择合适的色谱柱和内标物,关注标准使用气配制的湿度及平衡问题,并根据高沸点、高活性或极性物质的响应判断分析系统是否存在会对这些组分产生吸附作用的活点,否则将会对分析结果带来不良影响。
| [1] |
环境保护部. 环境空气挥发性有机物的测定罐采样/气相色谱-质谱法: HJ 759—2015[S]. 北京: 中国环境科学出版社, 2015.
|
| [2] |
段佳鹏, 梁胜文, 李蒲, 等. 武汉城区秋季大气挥发性有机物污染特征及部分物种来源的初步分析[J]. 环境监测管理与技术, 2017, 29(4): 23-27. DOI:10.3969/j.issn.1006-2009.2017.04.006 |
| [3] |
张璘, 孟晓艳, 秦玮, 等. 南京市臭氧、VOCs和PANs污染特征及变化趋势[J]. 中国环境监测, 2017, 33(4): 80-89. |
| [4] |
王荟, 高占啟, 赵艳, 等. 超低沸点挥发性有机物测定中的要点分析[J]. 环境监测管理与技术, 2019, 21(4): 46-48. DOI:10.3969/j.issn.1006-2009.2019.04.011 |
| [5] |
熊华竞, 王维康, 袁华明, 等. 加湿气体标准物质水含量分析[J]. 化学分析计量, 2021, 30(1): 7-12. DOI:10.3969/j.issn.1008-6145.2021.01.002 |
| [6] |
严静芬. 动态稀释法在汽车涂装行业固定污染源挥发性有机物测定中的应用[J]. 环境监控与预警, 2018, 10(3): 25-29. DOI:10.3969/j.issn.1674-6732.2018.03.006 |
| [7] |
李光辉, 蒋斌, 王思行, 等. 罐采样-预浓缩/气相色谱-质谱联用测定污染源废气中118种挥发性有机物[J]. 分析测试学报, 2020, 39(12): 1441-1450. |
| [8] |
王晖, 丁苗, 饶钦, 等. 全典型医化园区废气和环境空气中挥发性有机物污染特征[J]. 环境监控与预警, 2018, 10(6): 43-47. |
| [9] |
US EPA. Determination of VOCs in air collected in specially-prepared canisters and analyzed by GC/MS: Method TO-15a. [S/OL]. https://www.epa.gov/sites/default/files/2019-12/documents/to-15a_vocs.pdf.
|
 2022, Vol. 14
2022, Vol. 14 