2. 杭州蕙兰未来科技城学校,浙江 杭州 311121
2. Hangzhou Huilan Future Sci-tech City School, Hangzhou, Zhejiang 311121, China
20世纪80年代末,纳米技术作为一门新兴交叉学科逐渐发展,对21世纪的经济、国防和社会产生了重大影响[1]。纳米材料由纳米颗粒粒子组成,纳米颗粒(NPs)是指基本结构单元中至少有一维处于1~100 nm范围内的颗粒[2]。因其微小的粒径和特殊的空间结构,赋予其优越的反应活性、磁性、导电性及光学性质,被广泛应用于半导体材料、电子技术、能源开发、生物医药和环境保护等领域[3]。然而在纳米产品的生产、运输、使用或废弃过程中,纳米颗粒不可避免地被释放到自然环境中,并在大气、土壤及水体环境中进行迁移,与环境因素相互作用,可通过食物链对低级到高级生物产生不同程度的影响[3-4]。
水环境中,纳米颗粒物呈现一种稳定且分散的胶体体系,纳米颗粒可能会因为布朗运动而发生一系列的“聚集-分散-再聚集”或者“分散-聚集-再分散”等过程,最终因聚集体的粒径过大而沉降到沉积物上,或被水中浮游生物吞噬而逐级富集,最终影响纳米颗粒物在水中的生态毒性。因而纳米颗粒的毒性往往与其尺寸大小、化学组成、形状和表面物理化学性质等相关[5-6]。
随着现代科学分析技术的发展,对纳米颗粒表征的分析技术也逐渐成熟,主要包括扫描电子显微镜法、透射电子显微镜法、动态光散射技术、分光光度法和单颗粒-电感耦合等离子体质谱法(SP-ICP-MS)等,为纳米颗粒的研究提供了坚实的技术支撑[7]。现选用SP-ICP-MS法测定地表水中的金属纳米颗粒,对分析条件和影响因素进行初探。
1 单颗粒-电感耦合等离子体质谱法原理 1.1 分析原理SP-ICP-MS法是建立在电感耦合等离子体质谱法(ICP-MS)基础上的一种信号采集技术。当样品中的待测元素以溶解离子态稳定且均匀分布时,则单位时间内被检测到的响应值可被视为常数,即一个连续稳定的强度信号值[8]。当样品溶液中含有目标元素的纳米颗粒,元素在溶液中的分布不再均匀,当足够分散的纳米颗粒溶液雾化后进入等离子体形成气溶胶,会电离产生离子流,一个纳米颗粒对应一束离子流,这束离子流进入检测器后会在极短时间内被读取,并形成高于溶液基线背景信号的一个独立、不连续的极强脉冲信号[8]。用时间分辨模式采集数据,因纳米颗粒数量浓度与脉冲信号个数成正比,纳米颗粒粒径与脉冲信号强度成正比的关系,可同时获得纳米颗粒数量浓度与粒径的定量结果[8-9]。
1.2 颗粒数量浓度计算原理样品由进样系统经过雾化、离子化等最终进入检测器,在此过程中能被检测到的信号存在一定损失,这与样品提升量和传输效率有关[10],纳米颗粒数量浓度与脉冲信号个数成正比,关系公式见式(1)。
| $f_{\mathrm{NP}}=N_{\mathrm{NP}} \cdot Q_{\mathrm{sam}} \cdot \eta_{\mathrm{n}} $ | (1) |
式中:fNP——脉冲信号个数,个/min;NNP——纳米颗粒数量浓度,个/mL;Qsam——样品提升量,mL/min;ηn——传输效率。
ηn是关键参数,通过测定单位时间内的进样量得到Qsam,再采用已知NNP的纳米颗粒标准溶液进样,由软件计算获得fNP,通过式(1)标定ηn,作为校正参数代入公式,获得待测样品中的NNP。
1.3 颗粒粒径计算原理颗粒粒径与脉冲信号的强度成正比,需要将检测器在单位时间内测到的离子强度信号转换成纳米颗粒的质量信号[10]。进入仪器的有效离子质量(W)的计算公式见式(2)。
| $ W=\eta_{\mathrm{n}} \cdot Q_{\mathrm{sam}} \cdot t_{\mathrm{dwell}} \cdot C $ | (2) |
式中:tdwell——单位时间,ms;C——待测金属溶解态离子质量浓度,μg/L;ηn和Qsam同式(1)。
建立离子强度与质量强度的质量流量方程。在相同的测试条件下,得到溶解态离子标准曲线的信号响应值(S)。W与S呈线性关系,求得质量流量方程斜率(k)。净强度信号值与曲线斜率的比值为样品目标元素的质量[10],目标元素质量在颗粒中仅占一定百分比fm(若为单质金属纳米颗粒,则fm=1)。纳米颗粒的质量(mNP)计算公式见式(3)。
| $ m_{\mathrm{NP}}=\frac{S_{\text {pulse }}-S_{\mathrm{bkgd}}}{k \cdot f_m} $ | (3) |
式中:mNP——纳米颗粒的质量,μg;Spulse——纳米颗粒信号强度;Sbkgd——背景信号强度,包括仪器噪声、溶解态离子信号、检测不到的小粒径纳米颗粒信号等;k——质量流量方程斜率;fm——目标元素质量在颗粒中的百分比。
假设把每个纳米颗粒近似当作一个实心球体[10-11],则颗粒粒径大小(dNP)计算公式见式(4)。
| $ d_{\mathrm{NP}}=\sqrt[3]{\frac{6 m_{\mathrm{NP}}}{\pi \rho}} $ | (4) |
式中:dNP——纳米颗粒粒径大小,nm;π——圆周率;ρ——纳米颗粒的密度,kg/m3。
2 实验部分 2.1 仪器和试剂 2.1.1 仪器和参数采用NexION 2000G电感耦合等离子体质谱仪(美国珀金埃尔默公司),用标配调谐液(NexION Setup Solution)对仪器进行参数优化,具体参数见表 1。
| 表 1 电感耦合等离子体质谱仪参数 |
仪器调谐达到最佳状态后,进行单颗粒测试,驻留时间为50 μs,扫描时间为100 s,各元素参数见表 2。
| 表 2 各元素参数 |
以美国nano Composix公司生产的2种规格金纳米颗粒(AuNPs)为单颗粒标准溶液,分别为粒径30 nm(颗粒数量浓度为9.92×106个/mL)和粒径50 nm(颗粒数量浓度为9.89×106个/mL)。测试换算得到Qsam为0.282 mL/min,ηn为6.54。以多元素混合标准溶液(IS - 91131 - 1,美国AccuStandard公司)配制溶解态元素标准曲线。
2.2 样品采集与前处理采集某流域地表水,置于样品瓶中,在4 ℃冷藏条件下运送至实验室,于0~4 ℃低温保存。样品分析前用0.45 μm滤膜过滤,超声处理15 min,使溶液中颗粒足够分散。
3 结果与讨论 3.1 地表水中金属纳米颗粒数量浓度的测定分别测定地表水样品中银、钛、铜、锌、镉、铅6种金属纳米颗粒(AgNPs、TiNPs、CuNPs、ZnNPs、CdNPs、PbNPs)的数量浓度,平行测定3次,计算平均值和相对标准偏差(RSD),结果见表 3。由表 3可见,测定结果的精密度较好,RSD均<10%。其中AgNPs和CdNPs的颗粒数量浓度较高,CuNPs和ZnNPs的颗粒数量浓度较低。地表水中不仅含有溶解态金属离子,同时也含有纳米颗粒,各元素纳米颗粒数量浓度在2.00×103~1.92×106个/mL之间,呈现出较大的差异。
| 表 3 地表水中金属纳米颗粒数量浓度的测定(n=3) |
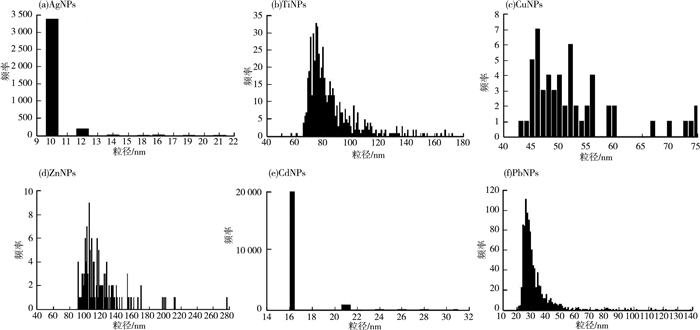
分别测定AgNPs、TiNPs、CuNPs、ZnNPs、CdNPs、PbNPs的粒径,结果见图 1(a)—(f)。
|
图 1 地表水中AgNPs、TiNPs、CuNPs、ZnNPs、CdNPs、PbNPs的粒径测定结果 |
由图 1可见,AgNPs和CdNPs的粒径分布相对单一且粒径较小,平均粒径为10和16 nm;其他4种纳米颗粒(TiNPs、CuNPs、ZnNPs和PbNPs)的粒径均在较广的范围内分布,粒径范围分别为58~176,43~75,90~278和19~136 nm,平均粒径分别为87,53,120和31 nm,占比最多的粒径分别为78,49,107和26 nm。
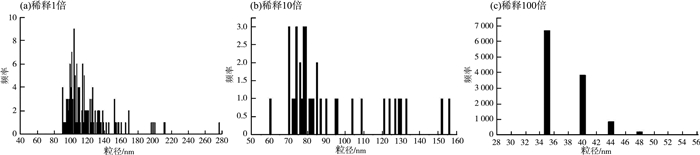
3.3 不同稀释倍数下ZnNPs的粒径分布和数量浓度对粒径分布最广的ZnNPs进行稀释后测定,稀释1,10和100倍时ZnNPs颗粒粒径分布范围见图 2(a)—(c)。
|
图 2 不同稀释倍数下ZnNPs的粒径分布 |
由图 2可见,随着稀释倍数的增加,颗粒粒径分布范围逐渐缩小,平均颗粒粒径和占比最多的颗粒粒径也在减小,并逐渐趋向于单一化,平均颗粒粒径依次为120,92和38 nm,占比最多的颗粒粒径依次为107,77和35 nm,同时颗粒数量浓度逐渐增加,依次为3.15×103,8.39×103和2.66×107个/mL,溶解态离子质量浓度依次为11.1,2.40和0.66 μg/L。
稀释后的颗粒数量浓度与稀释倍数不成比例,但也有逐级变化的趋势。这可能与纳米颗粒在水体中的运动状态有关,多个单一颗粒因布朗运动相互聚集或分散,导致2个或2个以上的颗粒聚集在一起,而被仪器当作一个大颗粒而读取信号,得到的结果颗粒粒径偏大,颗粒数量浓度偏小。因此样品中的纳米颗粒是否完全分散就尤为重要,需要再优化前处理方法和分析参数,同时缩小稀释倍数再次验证。此外,测定结果也与溶解态离子质量浓度有关,质量浓度过高会将基线背景拉高,抵消一部分纳米颗粒物通过而产生的信号,同时也会造成一些高信号值的误判断,因而可以在纳米颗粒标准溶液中加入不同质量浓度梯度的溶解态离子,进一步探究对其的影响。
4 结语采用SP-ICP-MS法测定地表水中的AgNPs、TiNPs、CuNPs、ZnNPs、CdNPs、PbNPs 6种金属纳米颗粒。结果表明,纳米颗粒数量浓度为2.00×103~1.92×106个/mL。在粒径分布上,AgNPs和CdNPs相对单一且粒径较小,平均粒径为10和16 nm;其他4种纳米颗粒(TiNPs、CuNPs、ZnNPs和PbNPs)的粒径均在较广的范围内分布,粒径范围分别为58~176,43~75,90~278和19~136 nm。但样品本身的性质、溶解态离子质量浓度、稀释倍数、分析时间、传输效率等也是影响测定结果的重要因素,需要再进一步优化样品的前处理过程,比如样品的超声时间和频率、分散剂的加入、颗粒分离技术、预处理后的静置时间等。此外,仪器分析中的驻留时间、读取时间等参数也需要进一步优化,以此增加SP-ICP-MS分析结果的准确性,更好地对纳米颗粒进行定量分析和表征。
| [1] |
吕继涛, 张淑贞. 环境中纳米材料的分离与分析方法[J]. 化学进展, 2012, 24(12): 2374-2383. |
| [2] |
陈泽璇, 钟汉杰, 肖杨, 等. 纳米颗粒与重金属污染对水生生物的生态毒理效应研究进展[J]. 广东化工, 2021, 48(6): 77-78. DOI:10.3969/j.issn.1007-1865.2021.06.038 |
| [3] |
刘振中, 邓慧萍, 陈战利. 纳米颗粒的危害及在水体中的去除研究进展[J]. 安全与环境学报, 2015, 15(4): 272-277. |
| [4] |
谭凌艳, 杨柳燕, 缪爱军, 等. 人工纳米颗粒对重金属在水生生物中的富集与毒性研究进展[J]. 南京大学学报(自然科学版), 2016, 52(4): 582-589. |
| [5] |
李国新, 赵超. 纳米材料在环境中的应用及生物毒性研究进展[J]. 四川环境, 2013, 32(2): 102-109. DOI:10.3969/j.issn.1001-3644.2013.02.022 |
| [6] |
杨艺, 张焕祯, 刘俊峰. 纳米颗粒在水环境中的团聚行为和毒性效应研究[J]. 环境工程, 2016, 34(9): 17-21. |
| [7] |
杨晓月, 程和发. 水体中金属(氧化物)纳米颗粒的环境行为与污染控制研究进展[J]. 环境化学, 2021, 40(2): 436-449. |
| [8] |
管鹏, 郭鹏然, 潘佳钏, 等. 基于单颗粒电感耦合等离子体质谱法测定环境基质水样中纳米银颗粒[J]. 分析测试学报, 2020, 39(5): 626-631. |
| [9] |
张春梅, 徐强, 杜静, 等. 单颗粒-电感耦合等离子体质谱测定海水中银纳米颗粒[J]. 分析化学, 2020, 39(5): 1260-1267. |
| [10] |
PACE H E, ROGERS N J, JAROLIMEK C, et al. Determining transport efficiency for the purpose of counting and sizing nanoparticles via single particle inductively coupled plasma mass spectrometry[J]. Analytical Chemistry, 2011, 83(24): 9361-9369. |
| [11] |
杨远, 龙晨璐, 杨兆光, 等. 纳米银的单颗粒-电感耦合等离子质谱法表征及其测定[J]. 分析化学, 2014, 42(11): 1553-1560. |
 2023, Vol. 15
2023, Vol. 15 

