2. 江苏省环境监测中心,江苏 南京 210019;
3. 江苏省生态环境评估中心,江苏 南京 210036;
4. 江苏省宿迁环境监测中心,江苏 宿迁 223809
2. Jiangsu Provincial Environmental Monitoring Center, Nanjing, Jiangsu 210019, China;
3. Jiangsu Ecological Assessment Center, Nanjing, Jiangsu 210036, China;
4. Suqian Environmental Monitoring Center Station, Suqian, Jiangsu 223809, China
地下水是重要的自然资源,在保证饮用水安全、区域经济发展和生态文明建设等方面起着不可替代的作用[1-4]。其中,地下水水质安全是保障其生态环境功能的前提[3, 5-7]。随着经济社会的发展,地下水环境压力与日俱增,地下水水质安全问题日益突出[8-12]。基于《全国地下水污染防治规划(2011—2020年)》《地下水管理条例》(2021年12月1日起施行)等相关要求,2015年前要全面建立地下水环境监管体系与地下水环境监测网络,对地下水进行动态监测,并用法律法规保障监测网的建设和运行,并确保地下水水质安全[8, 13]。
有研究发现,位于江苏省宿迁市中部的某监测井地下水连续3年砷(As)超标。As具有非常强的毒性,长期饮用高砷水会导致慢性砷中毒和癌症等疾病[14-15]。该监测井成井深度为37.3 m,监测目标层为区域第Ⅱ承压含水层,该含水层由中、早更新统松散砂层组成,水化学类型属HCO3--Ca2+·Mg2+(碳酸氢根钙镁)型水,水动力强度较小。参照《地下水质量标准》(GB/T 14848—2017)Ⅳ类限值[ρ(As)=0.05 mg/L],发现2018—2020年间该监测井ρ(As)最高超标1.94倍(2019年),且明显存在冬季As浓度高于夏季的特征。同步监测的其他水质参数则无明显的超标现象,且基本不呈现季节性特征。其中,pH值为7.14~8.08,平均值为7.51,为弱碱—碱性地下水;ρ(锰)超过Ⅲ类限值;ρ(铁)超过Ⅳ类限值;ρ(氟离子)、ρ(硫酸盐)和ρ(氯化物)总体上达到Ⅱ类水质标准。
探究该监测井As超标的原因,对于保障区域地下水生态环境安全及饮用水安全有重要意义。通过初步调查,该点位周边3 km范围内无工业企业分布,且宿迁地区其他监测点均不存在As超标现象,因此,初步认为该监测井As超标的主要原因可能与当地的岩性和地下水的环境相关。溯源调查中,有必要对该监测井附近的岩性、地下水中的As形态及其他环境指标等开展系统研究。有研究表明,地下水中As含量与含水介质中的吸附物质、碳酸盐、有机质和铁、锰物质有关,与氧化还原电位和酸碱度的关系尤为密切[16]。因此,对该监测井开展钻探工作,提取不同深度含水层中沉积物样品,进行地下水化学组成的测试,获取沉积物中不同形态的As含量,是摸清该监测井As超标原因的重要途径之一。
1 样品采集与测试 1.1 采集监测井地下水样品为进一步查明超标成因,在该监测井(以下简称“原井”)采集地下水样品,测试pH值、氧化还原电位、电导率、浑浊度、As、铁(Fe)、锰(Mn)、钾(K)、钠(Na)、钙(Ca)、镁(Mg)、铵根离子(NH4+)、氯离子(Cl-)、硫酸根离子(SO42-)、亚硝酸根离子(NO2-)、硝酸根离子(NO3-)、氟化物、硫化物、碳酸根离子(CO32-)、碳酸氢根离子(HCO3-)、总硬度和高锰酸盐指数、挥发性有机物和半挥发性有机物、石油烃等指标。
1.2 建设新井为便于精准对比,选取在原井能开展实际施工的最近位置建设同深度、同取水层位的水文地质钻孔,建设新井。经现场调查,新井位于原点位东侧5 m处。从区域水文地质条件角度,2个井位于同一个水文地质单元,新井位于区域流场下游,2个井揭露岩性组合一致,控制的地下水层位均为第Ⅱ承压含水层。判定2个井水力联系紧密,补径排条件一致,可以相互佐证。在新井同时采集地下水和沉积物样品,与原井样品数据开展对比。
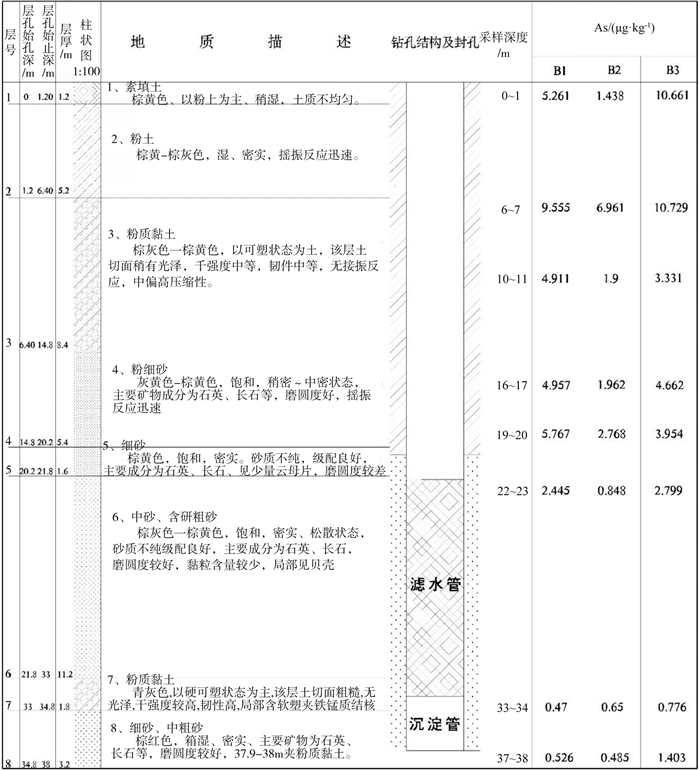
新井在勘探深度范围内的地基土层可分为8层。新井钻孔地层、成井结构示意见图 1。
|
图 1 新井钻孔地层、成井结构示意 |
根据岩性分布,分别于0~1,6~7,10~11,16~17,19~20,22~23,33~34,37~38 m采集8组沉积物样品,测试元素含量。根据欧洲共同体物质标准局提出的分步逐级提取法[17-18],研究沉积物样品中As及其他离子的3种不同重金属形态,即水溶态-可交换态-碳酸盐结合态(B1)、Fe-Mn氧化物结合态(B2)和有机物-硫化物结合态(B3)。
沉积物样品的测试步骤为:第1步(B1),称取样品1 g,加入40 mL的0.11 mol/L的乙酸(CH3COOH)溶液,放入MV680震荡搅拌仪(东莞睿思迈机电科技有限公司),设置温度为(22±5)℃,转速为30 r/min,震荡16 h;之后放入KS50R离心机(湖南凯达科学仪器有限公司)中开展固液分离,转速为4 000 r/min,时间为15 min,固液分离后,取出30 mL的上清液,过滤、待测;将剩余的残留物加入20 mL的去离子水清洗一遍,留待第2步使用。第2步(B2),将第1步残留物加入0.1 mol/L的盐酸羟胺(NH2OH·HCl)溶液40 mL,用2 mol/L的硝酸(HNO3)将pH值调至2,放入震荡搅拌仪,设置温度为(22±5)℃,30 r/min,震荡16 h;之后放入离心机中开展固液分离,设置转速为4 000 r/min,时间为15 min,固液分离后,取出30 mL的上清液,过滤、待测;将剩余的残留物加入20 mL的去离子水清洗一遍,留待第3步使用。第3步(B3),加入8.8 mol/L的H2O2(双氧水)溶液10 mL,在(22±5)℃条件下反应1 h,之后放入HH.S11-6电热恒温水浴锅(上海博迅医疗生物仪器股份有限公司)内,设置温度为(85±2)℃,消解1 h,之后重复加入8.8 mol/L的H2O2溶液10 mL,放入(85±2)℃的水浴锅消解1 h,再加入1 mol/L的乙酸铵(CH3COONH4) 溶液50 mL,用2 mol/L的HNO3将pH值调至2,放入震荡仪中,30 r/min,震荡16 h,之后放入离心机中开展固液分离,设置转速为4 000 r/min,时间为15 min,固液分离后,取出30 mL的上清液,过滤、待测。最后,将所有上清液取10 mL,蒸干后加10 mL 3% HNO3溶液后加盖,120 ℃加热溶解,之后过滤,留待仪器测试。
1.4 采集新井地下水样品并测试采用潜水泵进行洗井,洗井前对pH计(杭州丰控仪表有限公司)、YH100电导率和氧化还原电位仪(辽宁赛亚斯科技有限公司)等检测仪器进行现场校正并原位测试。洗井完成后2 h内采集地下水样品,并用0.45 μm滤膜过滤后用于分析主量元素(Ca、K、Mg等)和微量元素(As)。主量元素用电感耦合等离子体发射光谱仪(美国Teledyne Leeman Labs公司)测试,阴离子用ICs2000离子色谱仪(美国戴安公司)测试,微量元素用7700X电感耦合等离子体质谱仪(美国Agilent公司)测试,HCO3-和总硬度用碱度滴定盒滴定获得。测试项目包括As、铬(Cr)、Mn、铝(Al)、Ca、K、Mg、Na、硅(Si)、NH4+、SO42-、HCO3-、Cl-、氟离子(F-)、硫离子(S2-)、NO3-等。
2 结果与分析 2.1 水质结果分析原井样品中挥发性有机物和半挥发性有机物、石油烃等均未检出,符合点位周边无工业污染源分布的情况。原井和新井地下水监测结果见表 1。
| 表 1 原井和新井地下水监测结果 |
由表 1可见,原井ρ(As)为0.102 mg/L,是地下水Ⅳ类标准限值的2倍;新井ρ(As)为0.043 mg/L,低于Ⅳ类标准限值。因此,把新井监测数据作为区域的地下水本底值,用于原井As超标的原因分析。原井的ρ(Ca)、ρ(Mg)、ρ(SO42-) 明显高于新井,分别高出新井12%,15%,33%;原井氧化还原电位、ρ(Mn)、ρ(NH4+)、ρ(F-)分别低于新井33.7%,45.6%,62.9%,22.5%;原井pH值比新井高0.25,更偏碱性;原井电导率、ρ(Na)、ρ(Cl-)、ρ(HCO3-)、总硬度等指标分别比新井高出5%,5%,7%,8%和8%。
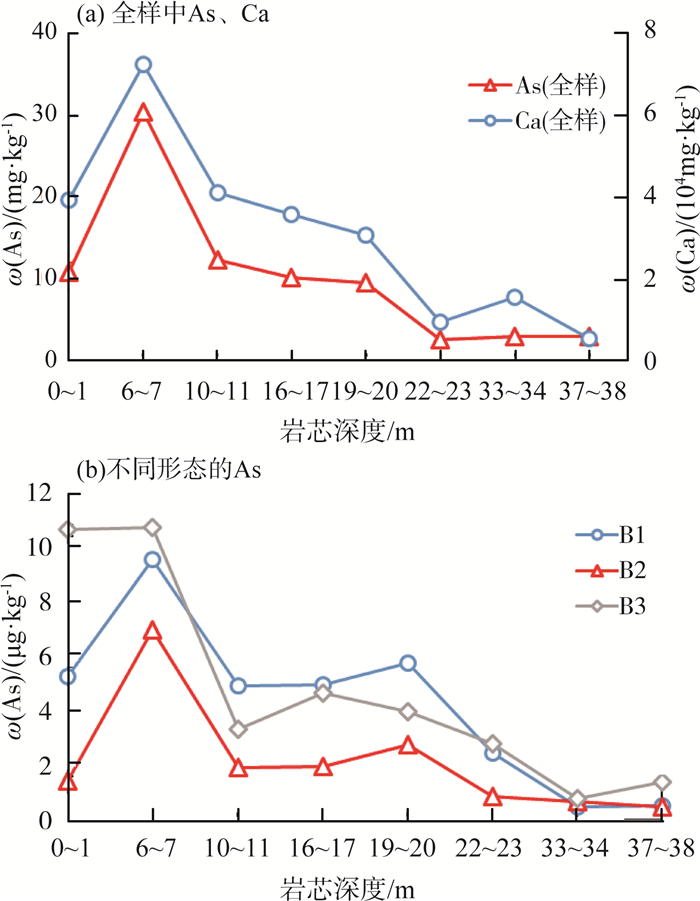
2.2 沉积物样品结果分析新井岩芯沉积物样品的全样中As、Ca质量分数与不同形态的As质量分数分布见图 2(a)(b)。由图 2可见,新井岩芯全样和不同形态的As质量分数均呈现出离地表越近其质量分数越高的趋势,均在6~7 m处最高,在33~38 m处为最低值。由图 2(a)可见,岩芯深度在6~7 m时,ω(As)为30 mg/kg;在37~38 m时,ω(As)为2.9 mg/kg。由图 2(b)可见,B1形态在岩芯深度为6~7 m时,ω(As)为9.555 μg/kg;在37~38 m时,ω(As)为0.512 μg/kg;B2形态在岩芯深度为6~7 m时,ω(As)为6.961 μg/kg,在37~38 m时,ω(As)为0.485 μg/kg;B3形态在岩芯深度为6~7 m时,ω(As) 为10.729 μg/kg,在37~38 m时,ω(As)为1.403 μg/kg。3种形态中,ω(As)在处于B1[ω(As)平均值为4.2 μg/kg] 和B3[ω(As)平均值为4.8 μg/kg)]2种形态时质量分数接近,而在B2[ω(As)平均值为2.1 μg/kg)]形态的质量分数最低。
|
图 2 新井岩芯沉积物全样中As、Ca质量分数分布与不同形态的As质量分数分布 |
沉积物分步提取的各元素不同形态测试结果见表 2。
| 表 2 沉积物分步提取的各元素不同形态测试结果 |
在自然环境下,As元素主要以无机氧化态As5+和还原态As3+存在[12, 15]。沉积物(土壤)中含砷矿物通常以砷酸盐、亚砷酸盐和硫化物等矿物相存在,在还原条件下,砷黄铁矿是砷的稳定宿主,其伴生砷与地下水砷分布高度相关[19]。在地下水中,砷主要以AsO42-(砷酸根)、H2AsO4-(砷酸氢根)和H3AsO3(砷酸)等形式存在[16]。前期研究发现[20],原生高砷地下水可分为以下几种类型:①还原性-中性/弱碱性高砷地下水(Ⅰ型),Ⅰ型地下水又可分为还原性-中性高砷地下水(Ⅰ-1型)和还原性-弱碱性高砷地下水(Ⅰ-2型);②氧化性-弱碱性高砷地下水(Ⅱ型);③氧化性-弱酸性高砷地下水(Ⅲ型)。即氧化还原电位(Eh)、pH值、地下水化学类型、沉积物中碳酸盐、有机质和铁、锰物质的变化影响沉积物As的吸附-解析过程,进而影响水体中As的浓度[16]。通过对比原井和新井中水化学组成与沉积物中不同形态As的分布,可有助于解释原井As超标的原因。
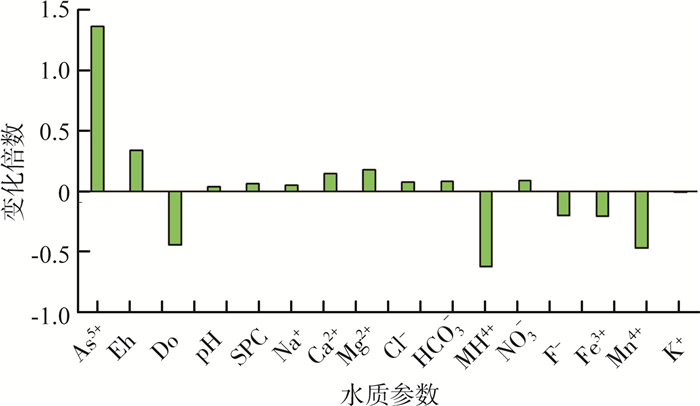
(1) 高pH值、还原性环境会促进沉积物中As的解吸和溶解,从而进入地下水形成积累[12, 15-16]。当地下水中的NO3-、SO42-发生了还原反应,这些还原可能在反硝化菌、硫酸根还原菌的作用下进行,而这些反硝化菌、硫酸根还原菌也可以作为As5+的电子受体,加速As5+向As3+的还原转化,导致As在地下水中加速释放。该监测井地下水属于还原性-中性/弱碱性高砷地下水(Ⅰ型)。地下水氧化还原电位为-114.2 mV,pH值为7.45,说明该井地下水环境处于还原性-弱碱性。还原性地下水中As形态以As3+为主,还原产物如ρ(Fe)、ρ(NH4+)等较高(0.007,0.63 mg/L);而水中氧化剂如ρ(NO3-)、ρ(SO42-)则较低(6.25,35.0 mg/L) (表 1)。原井相对于新井的水质参数变化倍数情况见图 3,结果显示原井的氧化还原电位比新井增加了0.34倍,表明原井比新井具有更强的还原环境。尽管原井和新井仅相距5 m,但原井相较于新井,其水化学组成更偏碱性,且具有更强的还原环境,这些均有助于As加速溶解释放到地下水中[12, 15-16],从而造成原井中As5+质量浓度高出新井1.36倍。此外,原井的Eh、pH值、电导率、ρ(Na+)、ρ(Ca2+)、ρ(Mg2+)等分别比新井增加了0.34,0.04,0.05,0.14和0.18倍。
|
图 3 原井相对于新井的水质参数变化倍数情况 注:变化倍数>0表示原井高于新井,<0表示原井低于新井。 |
(2) 地下水类型也会影响As的质量浓度[16]。研究发现[16],地下水化学类型从HCO3--Ca → HCO3--Mg → HCO3--Na → HCO3-·Cl-Na → Cl·HCO3--Na型转变时,地下水As质量浓度逐渐增加。原井中地下水阳离子以Na+(58.9 mg/L)、Ca2+(50.6 mg/L)和Mg2+(31.2 mg/L)为主,阴离子以HCO3-(356.9 mg/L)和Cl-(72.5 mg/L)为主,其他离子质量浓度较低(表 1),可以判断原井地下水类型为HCO3-Na·Ca·Mg型。这有利于地下水中的HCO3-与As反应生成稳定的As-HCO3-化合物,从而导致地下水中As的浓度增大[21]。特别是原井中ρ(Na+)、ρ(Ca2+)、ρ(Mg2+)较新井高出5%~18%,ρ(HCO3-)和ρ(Cl-)较新井高出7%~8%,加上弱碱性条件下,大部分矿物的表面带负电荷,促使地下水中的胶体及矿物质带更多的负电荷,Na+、Ca2+、Mg2+等阳离子质量浓度增大,降低了其对以HCO3-、PO43-、SO42-等阴离子形式存在的As的吸附能力,从而导致地下水中As的浓度增大。
(3) 沉积物中As的形态分布会随着地下水环境的改变从而影响地下水中As质量分数[22]。水溶态-可交换态-碳酸盐结合态(B1)是对地下水酸碱度和水化学最为敏感的成分[18]。水溶态和可交换态主要受沉积物的类型和地下水中As的质量分数控制,当地下水As质量分数高时,更多的As被吸附到黏土矿物等物质中,成为可交换态,反之亦然[22-23]。当地下水的pH值降低时,更易溶解沉积物中的碳酸盐,而当pH值偏碱性时,易从地下水中的Ca2+和HCO3-离子中再沉淀形成碳酸盐[24-26]。因此,酸碱度的变化也会对沉积物中B1形态的As产生影响。
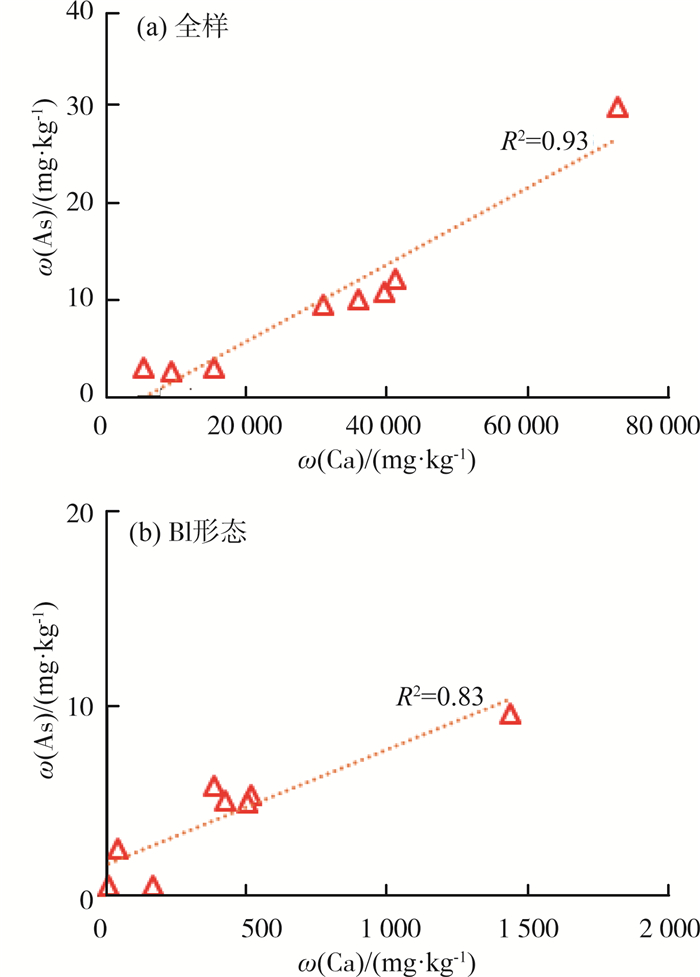
(4) 碳酸盐结合态是As的一个重要的形态。通过对沉积物全样和B1形态提取后发现,As质量分数和指示碳酸盐含量的Ca质量分数呈现非常好的相关性(R2>0.83)[图 4(a)(b)]。
|
图 4 新井沉积物全样和B1形态中As和Ca质量分数的相关分析 |
通过原井的季节性采样发现,夏季pH值相对较低,但仍处于弱碱性,因此仍然会导致碳酸盐的沉淀。由于夏季受亚洲季风控制,导致区域降水增多[27],土壤中溶解的Ca2+增多[28-29],导致地下水中输入了大量的Ca2+,当Ca2+进入地下水,在弱碱性环境下,加上夏季温度较高,导致碳酸钙溶解度下降,易发生沉淀[29-30],沉淀过程中吸附了As,降低了地下水As的质量浓度[16]。反之,冬季由于降水较少,土壤中输入的Ca2+较少,加上较低的温度,导致了沉积物中的碳酸盐易被溶解[29-30],释放了As,增加了地下水中As的质量浓度[16]。这与2018—2020年的季节性As监测数据一致,表现为夏季As质量浓度较低而冬季较高的特征。此外,原井与新井的对比也证实了这一推论,新井中不论Ca2+还是HCO3-浓度均低于原井,由于是同期取样,表明微环境的变化导致了新井中碳酸钙(CaCO3)的沉淀更多,移除了地下水中的Ca2+和HCO3-,同时也移除了As,降低了地下水中As的浓度。
(5) 高铁、锰的地质环境也能促进地下水中As的高赋值[16, 31]。地下水中固定砷酸盐的能力和含铁量呈正相关,HCO3-Ca·Mg型水在碱性条件下铁氧化物矿物对As的吸附性能随着pH值的升高而降低,铁氧化物矿物表面吸附的As被解吸附出来[16, 31]。但分步提取发现,Fe-Mn氧化物结合态中As质量分数较低,地下水一直处于还原环境,导致了高浓度的铁和锰离子。通过对比原井和新井可知,新井中ρ(Mn4+)为0.80 mg/L,比原井(0.44 mg/L)高出了近1倍,同时,新井氧化还原电位也比原井高出了0.36倍。如果Fe-Mn氧化物态的释放对监测井的As有较大贡献,那么新井中高浓度的Mn4+应该指示更多的Fe-Mn氧化物被还原,应释放更多的As,但实际情况是原井As质量分数比新井高,这表明Fe-Mn氧化物态的变化对地下水As质量分数的影响是有限的。
(6) 沉积物中的有机物和硫化物结合态的As也可能对原井地下水中高As有贡献[32-33]。有机物和硫化物是对地下水氧化还原状态非常敏感,当处于还原环境时,有机物和硫化物得以很好地保存,反之处于氧化环境时,有机物和硫化物分别被氧化为二氧化碳(CO2)和SO42-,同时释放As[34-35]。分步提取结果也发现,有机物和硫化物态中富含大量的As,当氧化还原状态改变的时候,有机物和硫化物态也会发生变化。但由于原井的氧化还原电位为-114.2 mV,处于一个较强的还原环境,在此情形下,有机质和硫化物较难被氧化释放出As。与新井的对比也说明,有机物和硫化物的氧化对As的贡献有限。由于新井的氧化还原电位更高,理应比原井氧化更多的有机物和硫化物,得到更高质量浓度的As,但事实是新井中As质量浓度反而较低。因此,有机物和硫化物态对原井中高As质量浓度的影响是有限的。
(7) 其他因素也会影响地下水中As的含量。一是成井工艺不规范造成串层污染。建井过程中,由于设备、工艺不规范或成井材料质量原因,可能会致使建井质量不合格,影响地下水水质;二是监测井年久已损。因建井时间较长,监测井可能已经受损,损坏的监测井亦会成为沟通不同含水层地下水的通道而造成串层污染;三是长期未洗井。深层承压水径流速度较小,地下水循环交替周期长,长期未洗井或洗井不充分可能造成底部淤积,同时影响地下水水质。
4 结论(1) 新井中地下水的ρ(As)为0.043 mg/L,未超过Ⅳ类标准限值,但同期测试的原井中的ρ(As)为0.102 mg/L,是Ⅳ类标准限值的2倍。
(2) 原井和新井中地下水均为还原性-弱碱性类型,地下水化学组成为HCO3- Na·Ca·Mg型。但两者的水化学组成存在显著差异,新井中地下水pH值、ρ(Na)、ρ(Ca)、ρ(Mg)、ρ(Cl-)、ρ(SO42-)、ρ(NO3-)、ρ(HCO3-)、总硬度均低于原井,其氧化还原电位、ρ(Mn)、ρ(NH4+)、ρ(F-)均高于原井。
(3) 原井所处的还原性-弱碱性的环境和受局部环境和气候影响的碳酸盐结合态的As是该井地下水中As超标的可能原因,而有机物-硫化物结合态与Fe-Mn氧化物结合态对地下水As超标的贡献则有限,但不能排除成井工艺不规范与监测井受到串层污染的影响。
| [1] |
夏军, 翟金良, 占车生. 我国水资源研究与发展的若干思考[J]. 地球科学进展, 2011, 26(9): 905-915. |
| [2] |
沈景文. 地下水与生态环境[J]. 干旱环境监测, 1990(2): 16-20. |
| [3] |
FALKENMARK M, FOLKE C, FOSTER S S D, et al. Groundwater: the processes and global significance of aquifer degradation[J]. Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences, 2003, 358: 1957-1972. DOI:10.1098/rstb.2003.1380 |
| [4] |
WANG Y X, ZHENG C M, MA R. Review: Safe and sustainable groundwater supply in China[J]. Hydrogeology Journal, 2018, 26(5): 1301-1324. DOI:10.1007/s10040-018-1795-1 |
| [5] |
姚金海. 论安全饮用水水权——兼论安全饮用水法的制定[J]. 经济与社会发展, 2021, 19(6): 63-76. |
| [6] |
唐克旺, 吴玉成, 侯杰. 中国地下水资源质量评价(Ⅱ)——地下水水质现状和污染分析[J]. 水资源保护, 2006, 22(3): 1-4, 8. |
| [7] |
白玉娟, 殷国栋. 地下水水质评价方法与地下水研究进展[J]. 水资源与水工程学报, 2010, 21(3): 115-119, 123. |
| [8] |
井柳新, 刘伟江, 王东, 等. 中国地下水环境监测网的建设和管理[J]. 环境监控与预警, 2013, 5(2): 1-4. |
| [9] |
SONG K, REN X, ADAM K M, et al. Research on drinking -groundwater source safety management based on numerical simulation[J]. Scientific Reports, 2020, 10(1): 15481. DOI:10.1038/s41598-020-72520-7 |
| [10] |
AHMED S E, AIDA D A, ALY I E, et al. Groundwater sustainability: a review of the interactions between science and policy[J]. Environmental Research Letters, 2020, 15(9): 093004. DOI:10.1088/1748-9326/ab8e8c |
| [11] |
FAMIGLIETTI J S. The global groundwater crisis[J]. Nature Climate Change, 2014, 4(11): 945-948. DOI:10.1038/nclimate2425 |
| [12] |
SCOTT F, HOLLY A M, ALEXANDER V G. Spatial and temporal variations of groundwater arsenic in South and Southeast Asia[J]. Science, 2010, 328(5982): 1123-1127. DOI:10.1126/science.1172974 |
| [13] |
井柳新, 刘伟江, 王东, 等. 浅谈我国地下水环境监测网的建设和管理[J]. 环境监控与预警, 2013, 5(2): 5-8. |
| [14] |
JACK C N, WANG J P, AMJAD S. A global health problem caused by arsenic from natural sources[J]. Chemosphere, 2003, 52(9): 1353-1359. DOI:10.1016/S0045-6535(03)00470-3 |
| [15] |
MOLLY T, MATHUROS R, PHILIP L. The developmental neurotoxicity of arsenic: cognitive and behavioral consequences of early life exposure[J]. Annals of Global Health, 2014, 80(4): 303-314. |
| [16] |
曾昭华, 张志良. 地下水中砷元素的形成及其控制因素[J]. 上海国土资源, 2003(3): 11-15. |
| [17] |
CHRISTINE M D, RHODRI P T, SHARON E M, et al. Evaluation of a sequential extraction procedure for the speciation of heavy metals in sediments[J]. Analytica Chimica Acta, 1994, 291(3): 277-286. |
| [18] |
THOMAS R P, URE A M, DAVIDSON C M, et al. Three-stage sequential extraction procedure for the determination of metals in river sediments[J]. Analytica Chimica Acta, 1994, 286(3): 423-429. |
| [19] |
许乃政, 龚建师, 檀梦皎, 等. 淮河流域高砷地下水的形成演化过程及其环境健康风险[J]. 中国地质, 2021, 48(5): 1418-1428. |
| [20] |
张迪, 郭华明, 倪萍, 等. 氧化还原条件对地下水中砷释放迁移的影响——以通榆县高砷地下水为例[J]. 第四纪研究, 2014, 34(5): 1072-1081. |
| [21] |
朱巍, 苏小四, 唐雯, 等. 松嫩平原地下水中氟、砷含量及其水化学影响因素[J]. 南水北调与水利科技, 2015, 13(3): 553-556. |
| [22] |
张连凯, 杨慧, 路国慧, 等. 秦皇岛河口沉积物砷形态分布特征[J]. 海洋科学, 2012, 36(9): 102-105. |
| [23] |
陈英, 孙英杰, 王芳芳, 等. 郑州北郊水源地沉积物中砷的含量及形态分布研究[J]. 青岛理工大学学报, 2013, 34(5): 55-59. |
| [24] |
DANIEL M D. The geochemistry of continental carbonates[J]. Developments in Sedimentology, 2010(62): 1-59. |
| [25] |
ALONSO Z, ANA M P. Palustrine carbonates[J]. Developments in Sedimentology, 2010(61): 103-131. |
| [26] |
KELTS K, HSV K J. Freshwater Carbonate Sedimentation. Lakes[M]. New York: Springer, 1978: 295-323.
|
| [27] |
马彬, 张勃. 基于格点数据的1961—2016年中国气候季节时空变化[J]. 地理学报, 2020, 75(3): 458-469. |
| [28] |
MENG X Q, LIU L W, WILLIAM B, et al. Dolomite abundance in Chinese loess deposits: A new proxy of monsoon precipitation intensity[J]. Geophysical Research Letters, 2015, 42(23): 10391-10398. |
| [29] |
AL NASSER W, SHAIKH A, MORRISS C, et al. Determining kinetics of calcium carbonate precipitation by inline technique[J]. Chemical Engineering Science, 2008, 63(5): 1381-1389. |
| [30] |
AGLAIA G X, EFTHIMIOS K G, PETROS G K. The precipitation of calcium carbonate in aqueous solutions[J]. Colloids and Surfaces, 1991, 53(2): 241-255. |
| [31] |
YU Z X, LI C X, WEI C, et al. Hydrothermal precipitation of arsenic in solution containing arsenic and iron based on scorodite formation[J]. Journal of Kunming University of Science and Technology(Natural Science Edition), 2017, 42(1): 1-8. |
| [32] |
KOLE S C, DCBNATH A, PRADHAN L. Organic matter and arsenic volatilising microorganism in mitigating arsenic toxicity of soil under legume-rhizobium symbiosis in Bengal Gram[J]. Indian Agriculturist, 2014, 58(3): 155-164. |
| [33] |
SIMONE B. The role of dissolved organic matter in arsenic mobilization in groundwaters of Bangladesh[D]. Boulder: University of Colorado at Boulder, 2010: 43-100.
|
| [34] |
HOSSAIN M A, JUNJI A, KAORI K, et al. Geochemical occurrence of arsenic in groundwater of Bangladesh: sources and mobilization processes[J]. Journal of Geochemical Exploration, 2003, 77(2): 109-131. |
| [35] |
JOHNNIE N M, WALTER H F, CAROLYN J. Partitioning of arsenic and metals in reducing sulfidic sediments[J]. Environmental Science & Technology, 1988, 22(4): 432-437. |
 2023, Vol. 15
2023, Vol. 15 

