苯甲醚是一种重要的有机合成中间体、医药中间体及精细化工产品,大量用于合成油脂生产中的抗氧化剂、塑料的稳定剂、农药和染料生产的初级原料、香料生产的优良溶剂。苯甲醚对人体皮肤、眼睛具有刺激性,甚至具有致突变性,其暴露途径有皮肤及黏膜吸收、吸入和摄入等。苯甲醚的生产和使用遍布我国主要流域沿岸,其对饮用水安全构成潜在危害[1]。
目前,国内还没有苯甲醚的国家或行业标准分析方法,仅在《生活饮用水标准检验方法有机物指标》(GB 5750.8—2022)[2]中规定了苯甲醚的限量值为0.05 mg/L。国内很多研究者对苯甲醚的前处理方法和检测方法进行了探究。赵慧琴[3-4]、韩嘉艺等[5]、王艳丽等[6]、李振国[7]都采用吹扫捕集-气相色谱质谱法对水体中的苯甲醚进行检测。对于无法使用吹扫捕集的情况,禹晓梅等[8]采用气相色谱法测定了非诺贝特原料药中残留的溶剂苯甲醚; 冯桂学等[9]采用顶空-气相色谱-质谱法测定苯甲醚,检出限低至0.005 μg/L; 彭鹭等[10]采用顶空固相微萃取-气相色谱质谱法对水中的苯甲醚进行测定,得到了0.012 μg/L的检出限。对于吹扫捕集-气相色谱质谱法,王艳丽等[6]和李振国[7]都发现,水体中的苯甲醚质量浓度在1~200 μg/L时线性不良,在20 μg/L时会出现拐点,为了避免这个问题,他们都采用了分段的工作曲线。冯桂学等[9]采用的气相色谱质谱法,不存在线性拐点问题,但所用仪器价格昂贵,且维护和使用成本都很高,难以大范围推广。彭鹭等[10]采用的方法能够得到很低的检出限,但前处理步骤过于复杂,线性范围很窄(0.05~0.50 μg/L)。因此,建立一种快速、准确、易行、可靠的水体中苯甲醚的前处理和检测方法具有十分重要的意义。
现参考并借鉴了上述研究者的成果,建立了顶空固相微萃取-气相色谱质谱法,对水体中的苯甲醚进行定性和定量测定。
1 实验部分 1.1 试剂和仪器试剂:甲醇(农残级,美国TEDIA公司); 苯甲醚、三氟溴苯(分析纯,上海菲达工贸有限公司); 抗坏血酸、盐酸(分析纯,国药集团上海化学试剂公司)。
仪器:Focus DSQ气相色谱质谱联用仪(美国Thermo Scientific公司); 电子分析天平(感量0.000 1 g,德国Sartorius公司); 固相微萃取手柄(美国Supelco公司); DB-5MS石英毛细管色谱柱(30 m×0.25 mm,膜厚0.25 μm,美国安捷伦公司); 100 μm PDMS、85 μm PA、65 μm PDMS/DVB、85 μm CAR/PDMS、50 μm CAR/PDMS/DVB萃取头(PDMS为聚二甲基硅氧烷,PA为聚丙烯酸酯,DVB为二乙烯苯,CAR为分子筛,美国Supelco公司); 15 mL顶空瓶; 5和25 mL容量瓶; 10和100 μL微量注射器。
1.2 溶液配制(1) 苯甲醚标准使用液:准确称取500 mg苯甲醚于25 mL容量瓶中,用甲醇配制成20.0 mg/mL的储备液。再用甲醇稀释成200 μg/mL的标准中间液,继续对标准中间液进行稀释,配成2 μg/mL的标准使用液。
(2) 内标使用液:用甲醇将三氟溴苯配制成20.0 mg/mL的储备液,再用甲醇稀释成100 μg/mL的内标中间液,继续对内标中间液进行稀释,配成10 μg/mL的内标使用液。
(3) 标准系列溶液:分别取10.0 mL去离子水于6个15 mL顶空瓶中,接着在每个顶空瓶中加入5 μL内标使用液,然后分别加入5,10,25,50,100和200 μL苯甲醚标准使用液,配制成1,2,5,10,20和40 μg/L的低质量浓度标准系列溶液。分别取10.0 mL去离子水于7个15 mL顶空瓶中,接着在每个顶空瓶中加入5 μL内标中间液,然后分别加入0.5,1,2,5,10,20和50 μL苯甲醚标准中间液,配制成10,20,50,100,200,500和1 000 μg/L的高质量浓度标准系列溶液。
1.3 实验条件 1.3.1 气相色谱条件柱温:60 ℃(保持2 min)~ 300 ℃(保持1 min),升温速度为30 ℃/min; 汽化室温度:250 ℃; 载气:高纯氦气(>99.999%); 载气流量:1.0 mL/min; 分流比:10 ∶ 1; 进样时间:3 min。
1.3.2 质谱条件电离源:电子轰击离子源(EI源,70 eV,230 ℃); 扫描方式:全扫描; 扫描范围:41~250 amu; 接口温度:250 ℃。
1.4 样品采集和保存根据《地表水和污水监测技术规范》(HJ/T 91—2021)对挥发性有机物分析的要求,采样前向样品瓶中加入抗坏血酸除去余氯,每100 mL样品加入50 mg的抗坏血酸。采集的水样用1.5 mol/L盐酸溶液调至pH值≤2。样品采集后冷藏运输,在4 ℃下保存,14 d内分析完毕。
1.5 实际样品分析取10.0 mL水样于15 mL顶空瓶中,根据苯甲醚质量浓度的不同分别加入5 μL三氟溴苯内标中间液(高质量浓度样品)或者5 μL三氟溴苯内标使用液(低质量浓度样品)。萃取头在气相色谱进样口老化5 min后,插入装有样品的顶空瓶,推出萃取头,在磁力搅拌的情况下顶空萃取一定时间,待吸附平衡萃取结束后收回萃取头。然后将萃取头插入质谱进样口3 min进行分析。
2 结果与讨论 2.1 萃取头的选择固相微萃取头的选择类似于选择毛细柱或液相柱,主要依据分析物质的分子质量(挥发性)与极性。分子质量小的化合物要选择膜厚的萃取头。苯甲醚分子质量小,在水中溶解度相对较低,挥发性较好,为了考察不同萃取头的萃取效果,分别选取了100 μm PDMS、85 μm PA、65 μm PDMS/DVB、85 μm CAR/PDMS和50 μm CAR/PDMS/DVB这5种萃取头。这5种萃取头的膜厚度差别不大,主要区别在于填料组成不同,有的是单一填料,有的是复合填料。
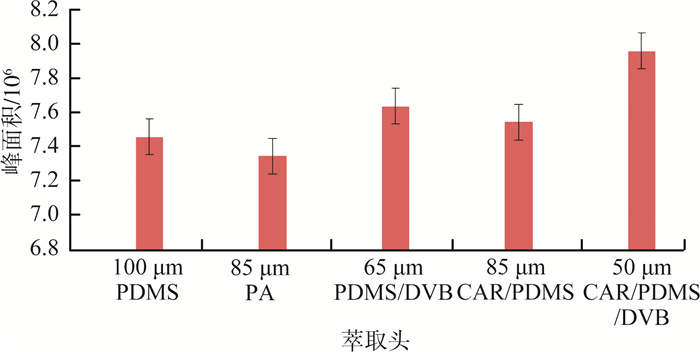
分别选用5种不同的萃取头对加标量为100 μg/L的苯甲醚水样进行实验,每个萃取头进行6次重复试验,取峰面积的平均值进行比较(图 1)。由图 1可见,50 μm CAR/PDMS/DVB的萃取能力强于另外4种。分析原因,PDMS萃取头擅长非极性挥发性化合物的萃取,而PA萃取头擅长强极性半挥发性化合物的萃取,而苯甲醚的极性不算强,但也不是非常弱,因此,PDMS萃取头和PA萃取头对苯甲醚的萃取效果相对较差; PDMS/DVB和CAR/PDMS这2种萃取头前者善于富集极性类化合物,后者善于富集小分子,对于苯甲醚都有较好的吸附效果; 而CAR/PDMS/DVB作为复合性最强的萃取头,结合了3种填料的优势,对苯甲醚显示出了最佳的吸附性能。因此选取50 μm CAR/PDMS/DVB萃取头进行实验。
|
图 1 不同萃取头对苯甲醚萃取能力的影响 |
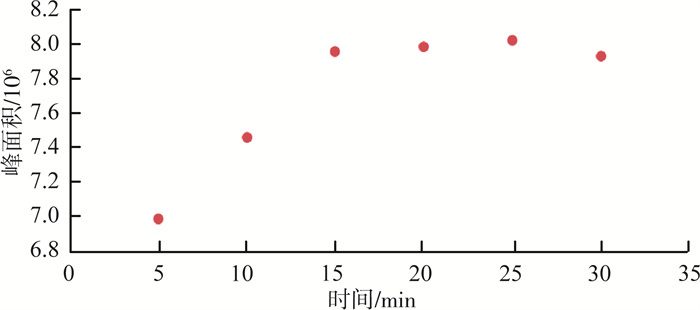
对加标量为100 μg/L的苯甲醚水样,采用50 μm CAR/PDMS/DVB进行萃取,萃取时间选取5,10,15,20,25和30 min,每个实验重复6次(图 2)。
|
图 2 不同萃取时间对苯甲醚萃取效率的影响 |
由图 2可见,萃取时间从5 min延长到15 min,吸附效果有明显增加,吸附时间达到15 min后,再增加吸附时间,吸附量基本没有变化,说明15 min时吸附已基本达到平衡,考虑到实验效率,因此选择15 min为萃取时间。
2.3 其他影响萃取效果的因素通常在样品进入气相色谱仪之前,要对样品进行改性,调整其pH值。但本实验的分析对象苯甲醚为中性,在采样时会利用盐酸将pH值调节成弱酸性,因此不必再对pH值进行调节。
为加快样品萃取速率,通常还会对分析样品进行搅拌,因此添加了搅拌子进行搅拌操作。需要特别注意的是,搅拌频率不一致会导致分析精度更差,因此保持搅拌频率恒定为300 r/min。
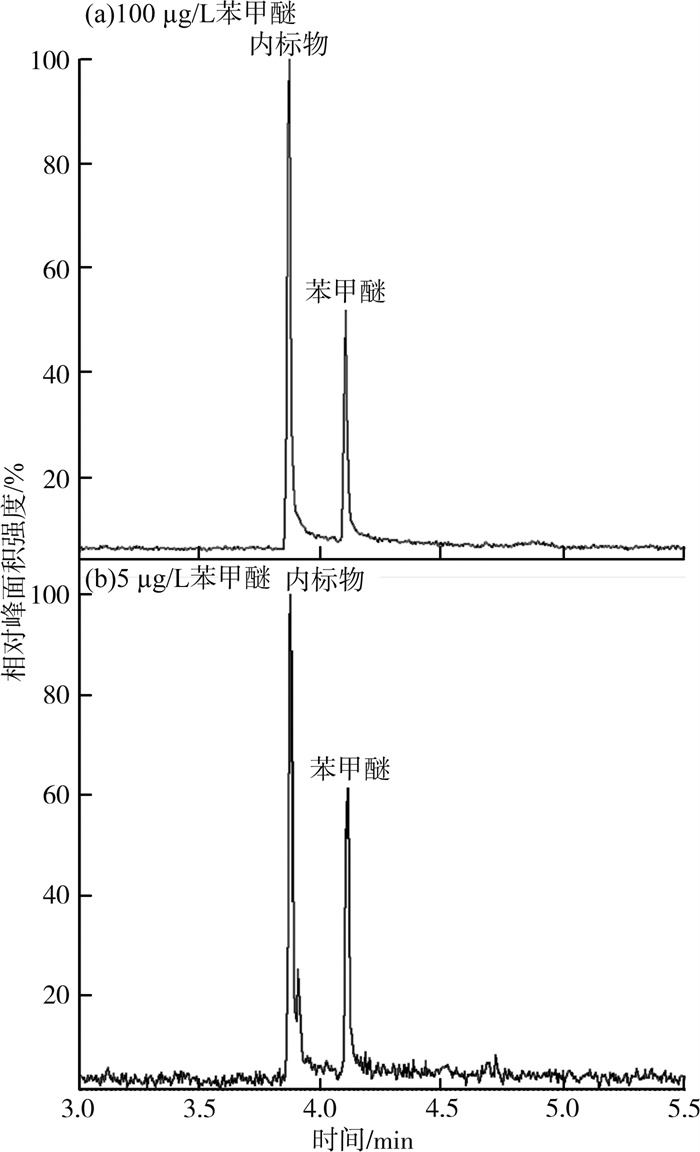
2.4 方法检出限和线性范围苯甲醚和内标物的特征离子流图见图 3(a)(b)。由图 3可见,内标物出峰时间和苯甲醚出峰时间间隔合理,完全没有干扰。
|
图 3 苯甲醚和内标物的特征离子流图 |
以苯甲醚的特征离子(65,78,108)峰面积和内标物的特征离子(81,131,210,212)峰面积比例为因子做工作曲线,结果见表 1。由表 1可见,经条件优化后,苯甲醚的测定线性范围为1~1 000 μg/L,线性相关系数均>0.999,可以满足实际水样的测定要求。为了考察本方法的检出限(MDL),重复测定1 μg/L的苯甲醚水样7次,根据公式MDL=t(n-1,0.99)× S,计算出该方法的最低检出限为0.3 μg/L。式中:t(n-1,0.99)=3.143,n=7,S为重复测定7次的标准偏差。检出限能够满足《GB 5750.8—2022》的限值要求(50 μg/L)。
| 表 1 不同质量浓度苯甲醚的工作曲线 |
在最优条件下,应用所建立的方法对10个实际水样进行测定,均未检出苯甲醚。为了验证方法的适用性,随机取其中1个水样进行加标回收实验,进一步考察方法的精密度和准确度。苯甲醚的加标量为10,60和300 μg/L,每个加标量平行测定6次,取平均值,结果见表 2。由表 2可见,根据低质量浓度工作曲线和高质量浓度工作曲线方法测定加标量为10 μg/L的样品时,内标物质量浓度为5和50 μg/L的结果一致性很强。实验结果的加标回收率为85%~120%,相对标准偏差(RSD)为3.95%~6.72%。说明该方法具有良好的精密度和准确度,适用于水中的微量及痕量苯甲醚残留的测定。
| 表 2 实际水样的苯甲醚加标实验结果(n=6) |
为了更加直观地对各种前处理方法进行比较,总结了液液萃取,吹扫捕集以及固相微萃取3种方法的优缺点,结果见表 3。由表 3可见,固相微萃取方法具有取样量少、分析时间短、不消耗有机试剂、线性范围宽及对环境友好等优点。
| 表 3 不同前处理方法测定苯甲醚的优劣比较 |
建立了顶空固相微萃取-气相色谱质谱法,对水中的苯甲醚进行定性和定量分析。实验结果表明,该方法分析时间短,只需要15 min,检出限低(0.3 μg/L),线性范围宽(1~1 000 μg/L); RSD≤6.72%,加标回收率为85%~120%,方法精密度和准确度均较好。该方法不需要复杂的前处理,所用仪器设备为实验室测定挥发性有机物的常用设备,测定条件和步骤简单,不需要使用有机溶剂,对环境友好,能够满足《GB/T 5750.8—2022》的要求,可应用于水中苯甲醚的分析测定。
| [1] |
张燕, 钱杰峰, 刘兰侠, 等. 水中苯甲醚的静态与动态顶空气相色谱分析方法建立及比较[J]. 中华预防医学杂志, 2013, 47(1): 542-544. |
| [2] |
中华人民共和国卫生部. 生活饮用水标准检验方法有机物指标: GB/T 5750.8—2022[S]. 北京: 中国标准出版社, 2022.
|
| [3] |
赵慧琴. 吹扫捕集/气相色谱-质谱联用法同时测定水中苯甲醚和8种苯系物[J]. 中国卫生检验杂志, 2014, 24(12): 1701-1703. |
| [4] |
赵慧琴, 刘斌, 张燕. 吹扫捕集/气相色谱-质谱法测定水中苯甲醚和8种苯系物的多组分分析方法验证[J]. 医学动物防治, 2015, 31(7): 818-820. |
| [5] |
韩嘉艺, 张振伟, 鲁波, 等. 饮用水中苯甲醚和8种苯系物的吹扫捕集-气相色谱-质谱联用测定法[J]. 环境与健康杂志, 2015, 32(3): 237-239. |
| [6] |
王艳丽, 赵志强, 崔连喜. 吹扫捕集/气相色谱-质谱法测定多种水样中的苯甲醚[J]. 中国给水排水, 2020, 36(18): 133-136. |
| [7] |
李振国. 吹扫捕集/气相色谱-质谱法测定水中的苯甲醚和甲基叔丁基醚[J]. 农业与技术, 2021, 41(16): 14-16. |
| [8] |
禹晓梅, 高苗苗. 气相色谱法测定非诺贝特原料药中残留溶剂苯甲醚的方法[J]. 北方药学, 2016, 13(1): 4-5. |
| [9] |
冯桂学, 刘莉, 王明泉, 等. 顶空-气相色谱-串联质谱法测定水中苯甲醚的含量[J]. 理化检验-化学分册, 2015, 51(12): 1721-1723. |
| [10] |
彭鹭, 杨创涛, 杨颖, 等. 顶空固相微萃取-气相色谱-质谱法检测饮用水中1, 2-二溴乙烯、苯甲醚和五氯丙烷[J]. 环保科技, 2020, 26(6): 48-53. |
 2024, Vol. 16
2024, Vol. 16 