2. 江苏科技大学,江苏 镇江 212003
2. Jiangsu University of Science and Technology, Zhenjiang, Jiangsu 212003, China
土壤重金属污染具有复杂性高、隐蔽性大、累积性强等特征[1],在浓度较低时难以检测,而且有些污染物需要长时间观察人畜健康状况后才能确定是否存在[2]。因此,开发灵敏度高、选择性强、抗干扰性强且简便快捷的土壤污染物检测方法具有重要意义。已报道的检测方法有原子吸收光谱法[3]、电感耦合等离子体发射质谱(ICP-MS)法[4]、电感耦合等离子体发射光谱(ICP-OES)法[5]、X射线荧光光谱(XRF)法[5]和荧光探针法[6-9]等。刘静等[10]采用全自动消解石墨炉原子吸收光谱法测定土壤中铅和镉,并对该方法的准确度和精密度进行分析,结果表明,全自动石墨消解过程无需人为看守,减少了对人的危害,原子吸收法分析土壤重金属结果精密度高,准确度好。梁凤玲等[11]采用电热板消解-ICP-MS法测定耕地土壤中的6种重金属,结果表明,电热板消解可以满足大批量样品同时消解,ICP-MS法可以同时测定多个元素,相对于原子吸收法,更加节省分析时间,检出限更低,精密度更好。杨华等[12]采用ICP-OES法测定水系沉积物中的6种重金属元素,结果表明,该方法可以同时测定多种元素,稳定性好,精密度高,相对于ICP-MS法,更加适合高浓度土壤样品的检测。刘玉纯等[13]采用粉末压片制样-XRF法分析土壤谱查样品测量条件的优化,结果表明,XRF法相对于传统湿法消解分析,节省了大量的前处理时间,压片速度快,可以做到大规模批量分析,适合大面积土壤普查研究,但是相比于ICP-OES法和ICP-MS法,其准确度和精密度略低。Luo等[14]报道了一种具有选择性的罗丹明荧光探针R1,该探针通过与钯离子(Pd2+)配位而起作用,可用于肉眼检测Pd2+,并通过紫外-可见荧光电喷雾电离质谱(ESI-MS)、核磁共振波谱(1H NMR)以及密度泛函计算(DFT),研究了Pd2+对探针的响应过程。此外,该探针成功地用于检测活细胞中的Pd2+。Li等[15]首次报道了一种用于铜离子(Cu2+)的新型有机硼荧光开启探针(BOPHY)。此探针显示非常弱的荧光,但是加入Cu2+时,该探针可以发出强荧光,对Cu2+的检测灵敏度高且选择性强,可用于稀释的人血清中Cu2+的检测,此外,该探针还在海拉细胞的Cu2+成像中得到应用。
原子吸收法、ICP-MS法、ICP-OES法和XRF法等方法虽然可以在一定范围内准确地检测大多数重金属离子,但也存在操作复杂、实验条件严格、测试时间长以及测试成本高等缺点。与这些方法相比,荧光探针是一种成本更低、操作更简便、选择性更强、灵敏度更高的分子工具,可以用于检测生物和环境中的重金属[16-17]。现建立了荧光探针PTAID以固态形式检测土壤中Pd2+和Cu2+的应用方法,并与传统的ICP-OES法进行比较,从反应时间、准确度、精密度等方面分析荧光探针法的优劣势,以期为土壤重金属污染物的检测提供数据支撑和技术支持。
1 实验部分 1.1 仪器与试剂仪器:UV-3010紫外分光光度计(日本岛津公司);PHS-25C型pH计(杭州奥立龙公司);BSA124S电子天平(德国赛多利斯公司);Spectofluorometer FS5荧光光谱仪(英国爱丁堡公司);Optima8000电感耦合等离子体发射光谱仪(美国Per-kinElmer公司);TOPEX全能型微波化学工作平台(上海屹尧仪器科技发展有限公司)。
试剂:4-羟乙基哌嗪乙磺酸(HEPES,98%,安耐吉化学);二甲基亚砜/水(DMSO/H2O) 溶液(V/V=3/2,pH值=7.4);HEPES缓冲液(0.2 mmol/L);探针PTAID溶液;硝酸(90%,Sigma-Aldrich);盐酸(36%,Sigma-Aldrich);氢氧化钠(98%,安耐吉化学);氢氟酸(40%,Sigma-Aldrich);双氧水(35%,Sigma-Aldrich);土壤底泥标准样品(GBW07456)。
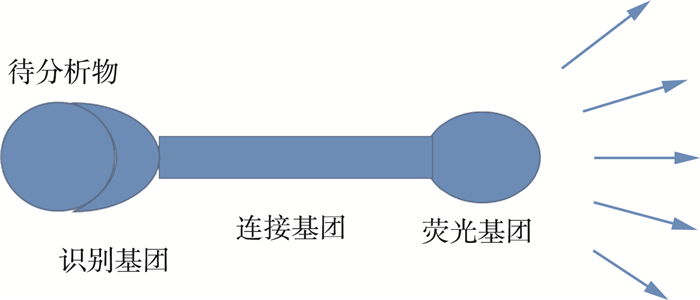
1.2 荧光探针PTAID的方法原理在某个系统中,当某种物质或某种特性发生变化时,荧光分子的荧光信号会发生变化,因此可以分析该物质的结构和性质。荧光探针通过探针与被检测物质结合前后荧光强度的变化来检测目标物质。荧光探针通常由荧光基团,连接基团和识别基团组成(图 1)。
|
图 1 荧光探针的组成 |
探针PTAID通过在DMSO/H2O溶液中的不同信号响应显示出对Pd2+和Cu2+具有高选择性和高灵敏度,并伴有明显的荧光“开-关”信号,且荧光颜色变化明显。
1.3 荧光探针PTAID的合成路线荧光探针PTAID合成路线见图 2。

|
图 2 荧光探针PTAID合成路线 |
将一些滤纸浸入PTAID(10 mmol/L)的DMSO溶液中30 min,干燥。随后,将滤纸置于不同浓度的Pd2+和Cu2+溶液中30 min,干燥。在365 nm紫外灯下可以观察到它们的荧光变化(图 3)。

|
图 3 不同浓度的Pd2+和Cu2+溶液下探针PTAID在试纸上的荧光照片 |
HEPES缓冲溶液:在100 mL蒸馏水中溶解0.238 g的HEPES,配置成浓度为10 mmol/L的HEPES缓冲溶液。
空白储备液:在500 mL烧杯中倒入300 mL的DMSO溶液、190 mL的蒸馏水和10 mL的HEPES缓冲溶液,配置成0.2 mmol/L的空白储备液,并用1.0 mol/L的盐酸溶液和1.0 mol/L的氢氧化钠溶液将其pH值调为7.4。
探针PTAID储备液:将探针PTAID溶解在DMSO溶液中,配置成1.0 mmol/L的探针储备液。
金属离子储备液:在蒸馏水中溶解各种金属离子的氯盐,如钠离子(Na+)、锌离子(Zn2+)、锡离子(Sn2+)、三价铁离子(Fe3+)、二价铁离子(Fe2+)、Pd2+、锰离子(Mn2+)、钙离子(Ca2+)、钡离子(Ba2+)、钾离子(K+)、镉离子(Cd2+)、镁离子(Mg2+)、钴离子(Co2+)、Cu2+、铬离子(Cr3+)、铝离子(Al3+)、碳酸铯(CsCO3)、硝酸银(AgNO3)以及硝酸铅[Pb(NO3)2],配置成3.0 mmol/L的金属离子储备液。
1.6 仪器工作条件ICP-OES测定的条件参数见表 1。Pd2+和Cu2+的观测波长分别为340.458和327.393 nm。
| 表 1 ICP-OES测定的条件参数 |
称取0.200 0 g左右烘干的土壤样品于聚四氟乙烯消解罐中,用水润湿,加入5.0 mL硝酸、2.0 mL氢氟酸和2.0 mL双氧水混合均匀,将内膜旋紧,置于全能型微波化学工作平台上消解。消解完成后,冷却至室温,取出消解内管放入赶酸板上,150~160 ℃消解赶酸至液体成近干,取下冷却,转移到50 mL容量瓶中,定容,待溶液澄清后,取上清液测试。用相同方法,制备全程序空白溶液。消解液采用ICP-OES仪测定。
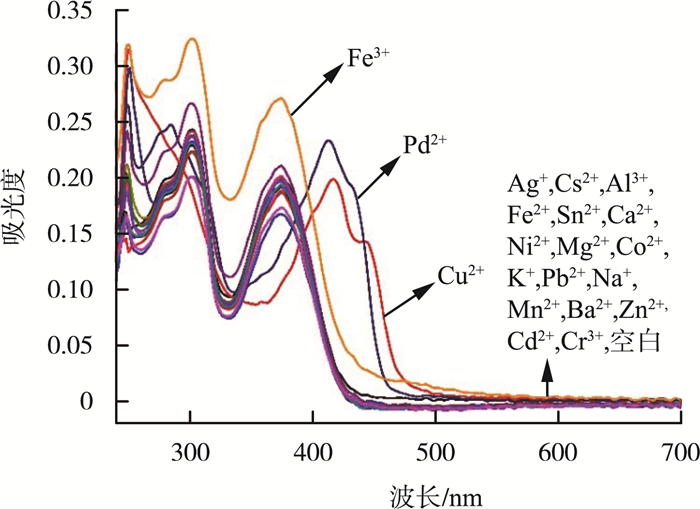
2 结果与讨论 2.1 紫外可见吸收光谱研究在5 mL的离心管中,加入3 mL的空白储备液、30 μL的探针PTAID储备液以及50 μL的金属离子储备液,得到含有不同金属离子的探针PTAID测试溶液,静置1 h后,在多种金属离子的存在下测试探针PTAID的紫外可见吸收光谱(图 4)。由图 4可见,探针PTAID在375 nm处具有较高的吸收峰,而在加入Pd2+或Cu2+时,PTAID的吸收峰明显发生了38 nm(从375到413 nm)和42 nm(从375至417 nm)的红移。同时在加入Pd2+或Cu2+后,可明显观察到探针PTAID溶液的颜色变化,而加入其他金属离子时,没有发生任何变化。因此,该探针可以用作Pd2+和Cu2+的比色探针。
|
图 4 加入不同金属离子时探针PTAID的吸收光谱 |
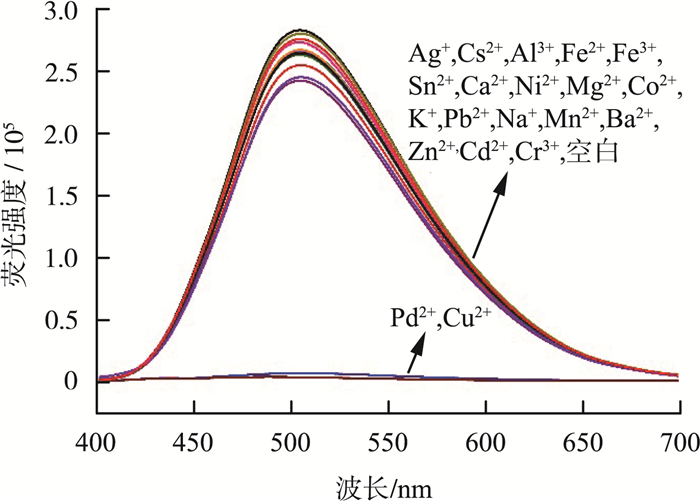
与其他竞争性金属离子相比,对Pd2+和Cu2+的高选择性对于评估探针PTAID的性能极为重要。加入不同金属离子时探针PTAID的荧光光谱见图 5。由图 5可见,探针PTAID在501 nm处显示强荧光,而当加入Pd2+和Cu2+时,探针PTAID的荧光被淬灭了,存在其他金属时,PTAID的荧光没有明显变化。结果表明,探针PTAID对Pd2+和Cu2+具有很高的选择性,可有效检测Pd2+和Cu2+。
|
图 5 加入不同金属离子时探针PTAID的荧光光谱 |
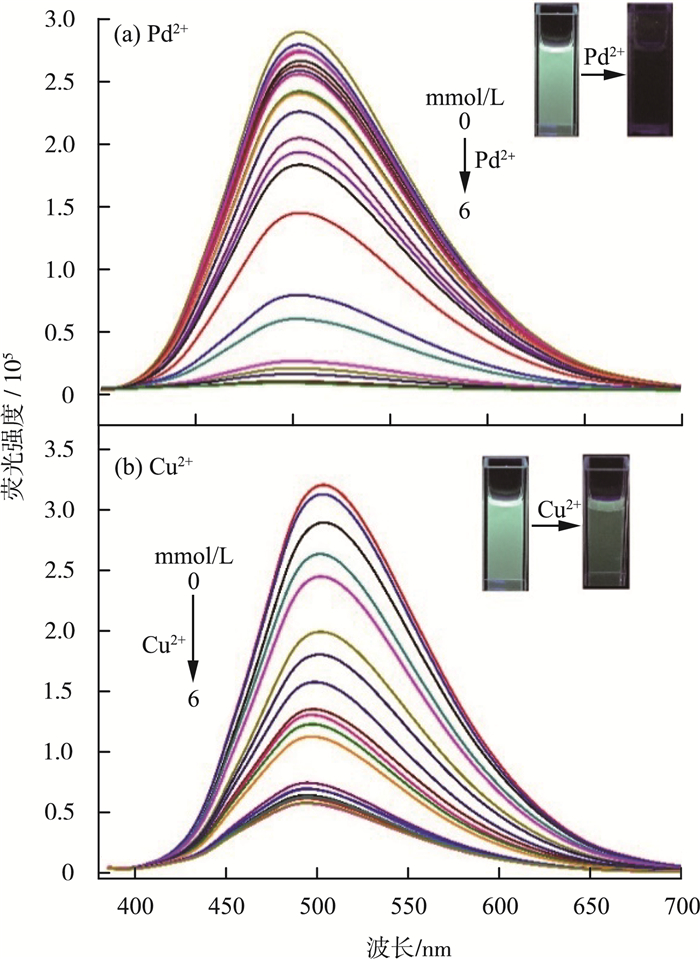
为了探究探针PTAID对不同浓度Pd2+和Cu2+荧光光谱的影响,在DMSO/H2O溶液中分别进行了荧光滴定,结果见图 6(a)(b)。由图 6可见,随着Pd2+或Cu2+浓度的增加,探针PTAID在501 nm处的荧光强度逐渐降低。此外,加入Pd2+或Cu2+时会使得探针PTAID溶液的荧光颜色从亮绿色变为无色或浅绿色。
|
图 6 探针PTAID对不同浓度Pd2+和Cu2+荧光光谱的影响 |
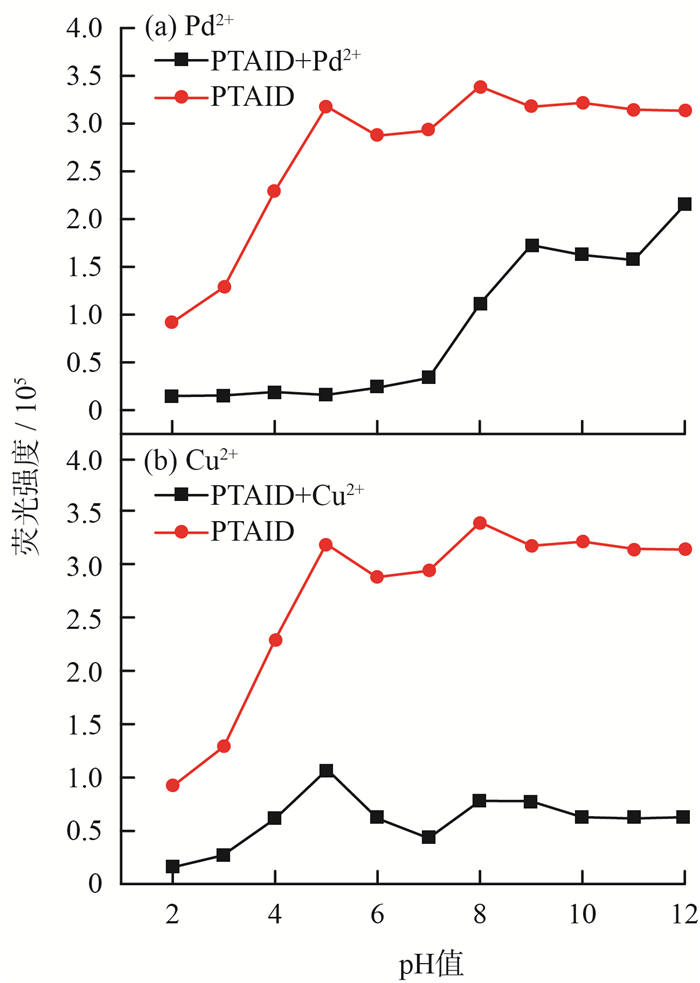
溶液pH值和反应时间对荧光体系测定结果的影响见图 7(a)(b)和图 8(a)(b)。
|
图 7 不存在Pd2+、Cu2+和存在Pd2+、Cu2+的情况下pH值对测定结果的影响 |
|
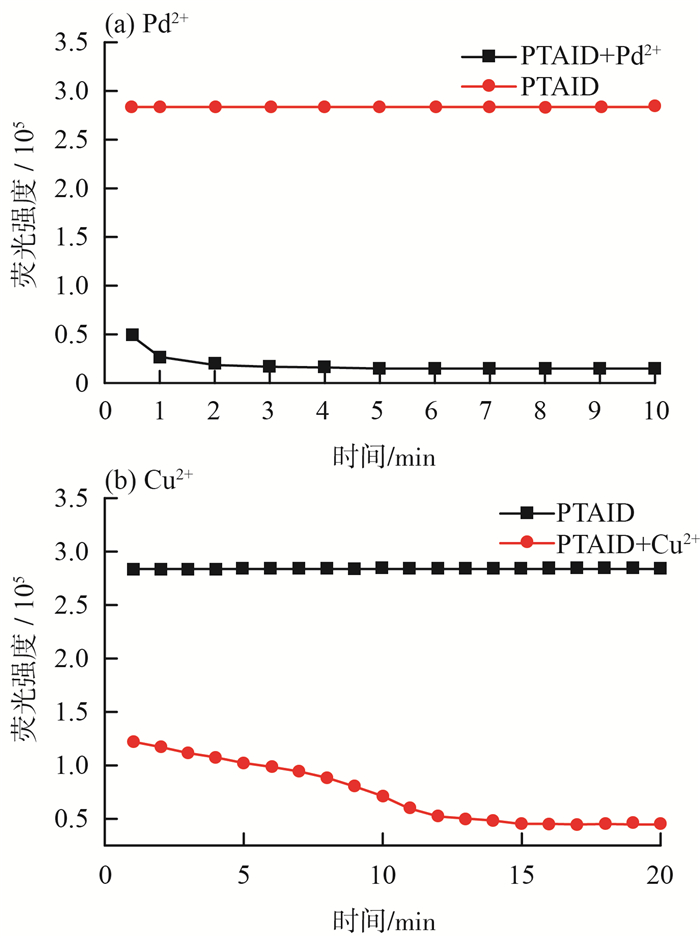
图 8 不存在Pd2+、Cu2+和存在Pd2+、Cu2+的情况下反应时间对测定结果的影响 |
由图 7可见,探针PTAID在pH值为4.0~12.0时,在501 nm处显示很高的荧光强度,说明该探针在从弱酸性到碱性的各种环境中显示出优异的稳定性。加入Pd2+后,探针PTAID在pH值为4.0~8.0范围内产生明显的荧光淬灭。加入Cu2+后,探针PTAID产生明显的荧光淬灭,并在pH值为4.0~12.0范围内保持稳定。结果表明,探针PTAID是可以在生物体内环境下检测Pd2+和Cu2+的新型荧光探针。
由图 8可见,探针PTAID在501 nm处显示很高的荧光强度,加入Pd2+后,在2 min内探针PTAID的荧光强度立即降低至最小并随后保持稳定。用同样的方法检测Cu2+,探针PTAID的荧光强度逐渐降低,并在15 min后达到最小值,且在测量时间内保持稳定。结果表明,探针PTAID可以快速检测Pd2+和Cu2+。
2.5 检出限的计算探针PTAID的荧光强度与Pd2+和Cu2+浓度的线性关系见图 9(a)(b)。由图 9(a)可见,在荧光增强区域取7个点,以C(Pd2+)为横坐标,501 nm处探针PTAID的荧光强度为纵坐标,进行线性拟合,得到直线方程y=12 079.928 57 x+104 587.142 86,决定系数(R2)=0.993 03。再测10组空白样,记录在501 nm处探针PTAID的荧光强度,计算标准偏差(SD)。根据Stern-Volmer方程LOD=3×SD/S计算检出限(S表示直线方程的斜率)。经计算,该探针对Pd2+的检出限为0.63 μmol/L。根据同样的方法,计算得到该探针对Cu2+的检出限为1.19 μmol/L。因此,即使在较低的浓度下,探针PTAID对Pd2+和Cu2+也显示出很好的灵敏度。

|
图 9 探针PTAID的荧光强度与Pd2+和Cu2+浓度的线性关系 |
ICP-OES法和荧光探针法的线性关系和检出限测定结果表 2。
| 表 2 ICP-OES法和荧光探针法的线性关系和检出限测定结果 |
由表 2可见,从线性关系上看,ICP-OES法更好,相关系数均≥0.999,从检出限来看,2种方法的检出限都远低于《土壤和沉积物12种金属元素的测定王水提取-电感耦合等离子体质谱法》(HJ 803—2016)要求[18]。
2.7 方法准确度比较称取0.200 0 g土壤底泥标准样品,分别用ICP-OES法和荧光探针法在选定的仪器条件下统一测定2种重金属的质量分数,结果见表 3。
| 表 3 ICP-OES法和荧光探针法的准确度测定结果(n=6) |
由表 3可见,ICP-OES法和荧光探针法得出的测定值结果均在标准参考值范围内,但荧光探针法更接近真值。这可能因为在酸消解条件下,土壤样品包裹了一部分重金属不能完全溶出,导致结果偏低。
2.8 方法精密度比较对实际土壤样品进行6次平行测试,测定精密度,结果见表 4。由表 4可见,2种重金属元素测定结果的相对标准偏差(RSD)为1.4%~3.4%,说明2种方法的精密度都较高,符合检测分析中的精密度要求。
| 表 4 精密度实验结果(n=6) |
本研究将荧光探针法和ICP-OES法进行比较研究,结果显示,探针PTAID对Pd2+和Cu2+有很高的灵敏度,检出限分别为0.63和1.19 μmol/L;通过条件优化实验,在pH值为4.0~12.0范围内,反应时间在0~15 min内可以快速检测Pd2+和Cu2+。与ICP-OES法相比,荧光探针法具有较高的准确度和精密度,分析结果均符合《HJ 803—2006》要求。相较于ICP-OES法,荧光探针法省去了复杂的酸消解时间,响应时间短、灵敏度高、选择性好。运用小分子荧光探针检测土壤中的重金属,可以做到快速定性和精准定量,在土壤重金属检测方面具有广阔的应用前景。
| [1] |
杨富斌, 穆晋, 马玖彤, 等. 荧光探针在土壤污染物检测中的应用研究进展[J]. 分析化学评述与进展, 2022, 50(8): 1131-1142. |
| [2] |
HUO B, DU M, GONG A, et al. A novel intramolecular cyclization-induced fluorescent "turn-on" probe for detection of Pd2+ based on the Tsuji-Trost reaction[J]. Analytical Methods, 2018, 10: 3475-3480. DOI:10.1039/C8AY00965A |
| [3] |
李飞飞, 翁文静, 张睿. 原子吸收光谱法在土壤环境监测中的应用[J]. 科学技术创新, 2018(29): 46-47. |
| [4] |
马莉, 司晗. 微波消解样品-电感耦合等离子体质谱法同时测定土壤中重金属元素和稀土元素[J]. 环境科学导刊, 2016, 35(2): 88-91. |
| [5] |
黄阳晓. 对比等离子发射光谱法/原子荧光法探讨便携式X射线荧光光谱法在测定土壤重金属中的应用[J]. 广东化工, 2016, 43(13): 261-263. |
| [6] |
YUAN Y H, TIAN M Z, WANG J L, et al. Development and cell imaging applications of a novel fluorescent probe for Cu2+[J]. RSC Advances, 2015, 85: 69453-69457. |
| [7] |
WANG Y, LIU S, CHEN H, et al. A novel "turn-on" fluorescence probe based on azoaniline-arylimidazole dyad for the detection of Cu2+[J]. Dyes and Pigments, 2017, 142: 293-299. DOI:10.1016/j.dyepig.2017.03.051 |
| [8] |
ASSIRI M A, AL-SEHEMI A G, PANNIPARA M. AIE based "on-off" fluorescence probe for the detection of Cu2+ ions in aqueous media[J]. Inorganic Chemistry Communications, 2019, 99: 11-15. DOI:10.1016/j.inoche.2018.11.001 |
| [9] |
WANG Y, ZHU Z, FAN C, et al. A naphthalene-dansylhydrazine based ratiometric fluorescence probe for selectively detecting Cu2+[J]. Tetrahedron Letters, 2020, 61: 151427-151430. DOI:10.1016/j.tetlet.2019.151427 |
| [10] |
刘静, 王利红, 王霞, 等. 全自动消解石墨炉原子吸收光谱法测定土壤中Pb和Cd[J]. 山东科学, 2013, 26(5): 15-17, 28. |
| [11] |
梁凤玲, 章雪明, 黄芳, 等. 电热板消解-ICP-MS法测定耕地土壤中6种重金属元素[J]. 现代农业科技, 2018(5): 183-184. |
| [12] |
杨华, 张永刚. 电感耦合等离子体原子发射光谱法(ICP-OES)测定水系沉积物中6种重金属元素[J]. 中国无机分析化学, 2014, 4(1): 22-24. |
| [13] |
刘玉纯, 林庆文, 马玲, 等. 粉末压片制样-X射线荧光光谱法分析地球化学调查样品测量条件的优化[J]. 岩矿测试, 2018, 37(6): 671-677. |
| [14] |
LUO W, LEI M, WANG Y, et al. An indole-rhodamine-based ratiometric fluorescent probe for Pd2+ determination and cell imaging[J]. Analytical Methods, 2019, 11: 1080-1086. DOI:10.1039/C8AY02508H |
| [15] |
LI Y, ZHOU H, YIN S, et al. A BOPHY probe for the fluorescence turn-on detection of Cu2+[J]. Sensor Actuator B Chemical, 2016, 235: 33-38. DOI:10.1016/j.snb.2016.05.055 |
| [16] |
CHEN X, WANG F, HYUN J Y, et al. Recent progress in the development of fluorescent, luminescent and colorimetric probes for detection of reactive oxygen and nitrgen species[J]. Chemical Society Reviews Journal, 2016, 45: 2976-3016. DOI:10.1039/C6CS00192K |
| [17] |
QIAN X, XU Z. Fluorescence imaging of metal ions implicated in diseases[J]. Chemical Society Reviews Journal, 2015, 44: 4487-4493. DOI:10.1039/C4CS00292J |
| [18] |
中华人民共和国环境保护部. 土壤和沉积物12种重金属元素的测定王水提取-电感耦合等离子体质谱法: HJ 803—2016[S]. 北京: 中国环境科学出版社, 2016.
|
 2024, Vol. 16
2024, Vol. 16 