2. 江苏省水产质量检测中心,江苏 南京 210017;
3. 上海爱博才思分析仪器贸易有限公司,上海 200335
2. Aquatic Product Quality Inspection Center of Jiangsu Province, Nanjing, Jiangsu 210017, China;
3. Shanghai AB Sciex Analytical Instrument Trading Co. Ltd., Shanghai 200335, China
目前用于抗焦虑、失眠、惊厥等病症的镇静剂主要有苯二氮卓类和吩噻嗪类2大类,能够使患者镇静,促进睡眠,其在人体内代谢缓慢,长期摄入后,会导致肝脏负担加重,记忆退化,运动神经等功能受到抑制[1-4]。近年来,我国多个省份水产品中检出地西泮(苯二氮卓类)残留[5-7],根据农业农村部2021年国家农产品质量安全监督抽查,11批次不合格水产品中有9批次检出地西泮。目前养殖水体及水产品中检出地西泮等镇静剂,其来源主要有养殖环节、流通环节、环境污染和其他来源等,或者上述多种来源叠加或交叉引入,其中养殖环节引入主要包括饲料、鱼药等投入品的隐性添加;流通环节引入主要包括运输环节非法添加,以降低水生动物对环境的应激反应来提高存活率[8-9];环境污染引入主要包括周边养殖的畜禽类动物的代谢物进入养殖环境中;其他来源引入主要包括垂钓行为中投放的钓饵、窝料和添加剂等。Brodin等[10]在瑞典部分地表水中检出奥沙西泮,质量浓度为0.58~0.73 μg/L,同时河里鲈鱼肌肉中奥沙西泮的质量浓度是水体中的近6倍。国内对养殖水体中的镇静剂残留检测技术研究较少,因此建立养殖水体中多种镇静剂残留的快速准确测定方法,为测定水体中的镇静剂及探讨其来源提供参考。
目前,镇静剂类药物残留的检测方法主要有酶联免疫(ELISA)法[11]、气相色谱-质谱联用(GC-MS/MS)法[12-15]、液相色谱(HPLC)法[16-17]、液相色谱-串联质谱(LC-MS/MS)法[18-22]。其中LC-MS/MS法具有灵敏度高、选择性好、抗干扰能力强等优点,成为目前测定镇静剂类药物的首选检测方法。该方法多应用在检测动物源性食品中镇静剂类药物残留[23],而对检测水体中镇静剂残留的报道较少。张力群等[24]建立了超高效液相色谱-串联质谱法同时测定水中5种苯二氮卓类镇静剂药物,定量限为0.3~1.3 ng/L,该研究主要针对苯二氮卓类镇静剂,且仅选择了地西泮-D5作为5种镇静剂的内标物,具有一定的局限性;张昕等[25]采用固相萃取-超高效液相色谱-串联质谱法测定水中5种常见的苯二氮卓类药物,外标法定量,定量限为0.05~0.5 ng/L,该研究未考虑复杂水样的基质效应对检测结果的影响。
现进一步优化了前处理条件和仪器分析条件,并利用同位素稀释方法校正实际样品的基质效应,建立了灵敏度高、准确度高的LC-MS/MS法,可同时测定养殖水体中23种镇静剂残留。
1 实验部分 1.1 仪器与试剂仪器:Triple Quad 5500超高效液相色谱-四极杆质谱联用仪(美国SCIEX公司);Agilent InfiniityLab Poroshell 120 SB-C18色谱柱(2.1 mm×100 mm,2.7 μm,美国Agilent公司);Allegra X-30R高速台式冷冻离心机(美国Beckman Coulter公司);Turbo Vap LV全自动氮吹浓缩仪(瑞典Biotage公司);DMT-2500涡旋混合器(常州金坛良友仪器有限公司);Milli-Q纯水仪(德国Merck公司);24位固相萃取装置(美国Supleco公司);Oasis HLB固相萃取小柱、Oasis MCX固相萃取小柱、C18固相萃取小柱(均为500 mg/3 mL,美国Waters公司)。
试剂:23种镇静剂及23种同位素内标物的质谱参数见表 1。其中序号1—14的镇静剂属于苯二氮卓类,质量浓度均为1.0 g/L,同位素内标物质量浓度均为100 mg/L,均购自美国Cerilliant公司;序号15—23的镇静剂属于吩噻嗪类,纯度>97%,购自德国Dr. Ehrenstorfer公司;序号18和20的同位素内标物纯度>99%,购自加拿大CDN公司;序号15—17,19,21—23的同位素内标物纯度>98%,购自德国WITEGA公司;甲醇、乙腈(色谱纯,德国Merck公司);甲酸(色谱纯,美国Tedia公司)。
| 表 1 23种镇静剂及23种同位素内标物的质谱参数① |
23种镇静剂标准储备液:对于苯二氮卓类镇静剂,移取适量的液体标准品溶解于甲醇并定容至50 mL;对于吩噻嗪类镇静剂,称取适量的固体标准品溶解于甲醇并定容至50 mL。23种镇静剂储备液的质量浓度为100 mg/L,23种同位素内标物储备液质量浓度为50 mg/L,分别于4 ℃避光保存。
混合标准工作液:分别移取适量各标准储备液,用甲醇/水(V ∶ V=1 ∶ 1)定容至10 mL。23种镇静剂混合标准工作液质量浓度均为1 mg/L,23种同位素内标物混合标准工作液质量浓度为100 μg/L,分别于4 ℃避光保存。
1.2.2 样品前处理水样均采集自各个养殖场的养殖池塘塘口,养殖水样的采集严格按照《水质采样技术指导》(HJ 494—2009)[26]执行。各养殖场的养殖水体pH值均为6.5~8.5。1 L养殖水样经0.45 μm尼龙滤膜过滤后,加入200 μL内标物混合标准工作液,以5 mL/min的速度过HLB柱(使用前依次用5 mL甲醇和5 mL超纯水活化),再用6 mL超纯水淋洗,真空抽干后,用5 mL乙腈洗脱,收集于10 mL离心管中。洗脱液在50 ℃下氮吹至近干,用50%的甲醇水(V/V)定容至1 mL,过0.22 μm滤膜,待上机检测。
1.2.3 色谱条件色谱柱柱温:35 ℃;流速:0.4 mL/min;进样量:2.0 μL。流动相A:0.1%甲酸水溶液;流动相B:乙腈。梯度洗脱:0~3.0 min,5%B;3.0~8.0 min,5%~60%B;8.0~10.0 min,60%B;10.0~11.0 min,60%~5%B;11.0~16.0 min,5%B。
1.2.4 质谱条件电喷雾电离(ESI)源,正离子扫描;扫描方式:多反应监测模式(MRM);喷雾电压:5 500 V;离子源温度:350 ℃;气帘气压力:379.21 kPa;离子源气1压力:379.21 kPa;离子源气2压力:379.21 kPa;射入电压:10 V;碰撞室射出电压:9 V;其他质谱采集参数见表 1。
2 结果与讨论 2.1 质谱条件与液相色谱条件的优化苯二氮卓类和吩噻嗪类镇静剂分子中均含有氮原子,在ESI离子模式下易与氢离子结合形成[M+H]+,故选择ESI+模式扫描。本研究在ESI+模式下将质量浓度为50 μg/L的23种镇静剂及23种内标物溶液,以连续注射的进样方式确定目标物的母离子,采用子离子扫描模式进行二级质谱分析,选择干扰小、信噪比大的离子对作为定量定性离子对,优化碰撞能量、去簇电压等质谱参数,优化后的其他质谱采集参数见表 1。
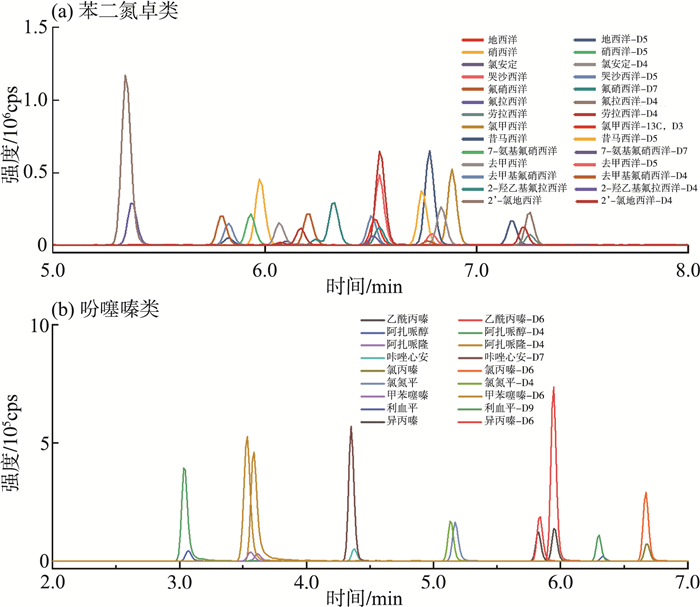
苯二氮卓类和吩噻嗪类镇静剂均属于极性化合物,易溶于甲醇、乙腈等有机溶剂,同时为弱碱性化合物[23],加入甲酸、乙酸铵等有助于目标化合物离子化,提高信噪比,因此考察了色谱柱在0.1%甲酸水溶液-乙腈、0.1%甲酸水溶液-甲醇、5 mmol/L乙酸铵溶液-乙腈、5 mmol/L乙酸铵溶液-甲醇等流动相体系下的分离效果。结果显示,色谱柱在0.1%甲酸水溶液-甲醇流动相体系下采用梯度洗脱对23种镇静剂及23种内标物具有较好的分离度,色谱峰形尖锐,且均能在3~8 min出峰(图 1)。
|
图 1 23种镇静剂及23种内标化合物的提取离子流色谱图 |
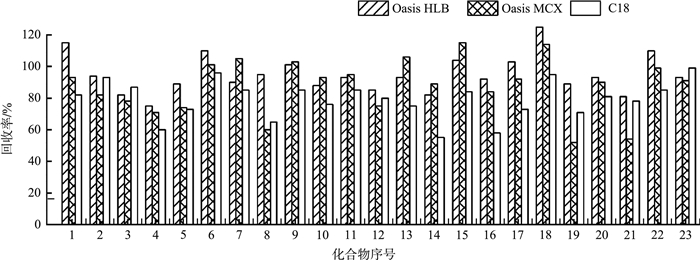
固相萃取(SPE)技术采用选择性吸附、选择性洗脱的方式对样品进行富集、分离、纯化,与传统的液液萃取法相比,可以提高分析物的回收率,更有效地将分析物与干扰组分分离,减少样品预处理过程,操作简单、省时、省力,是目前水质检测中常用的富集净化方法。本实验在优化了Oasis HLB柱、C18柱、Oasis MCX柱3种固相萃取柱的基础上,考察了这3种小柱的净化效果(平行测定6次),结果见图 2(化合物序号同表 1,下同)。由图 2可见,Oasis MCX柱对劳拉西泮、氯丙嗪、氯氮平、异丙嗪等目标化合物的净化效果较差,回收率<70%;C18柱对劳拉西泮、奥沙西泮、2′-氯地西泮、阿扎哌隆等目标化合物的净化效果较差,回收率<70%;Oasis HLB柱对目标化合物的回收率达到70%~125%,样品净化效果良好,能够减少目标化合物的损失。这是由于Oasis HLB柱填料是亲水-亲脂聚合物,镇静剂类极性物质在Oasis HLB柱上能被更好地净化,灵敏度和选择性均较高,因此选择Oasis HLB柱对样品进行前处理。
|
图 2 不同固相萃取小柱对样品提取液的净化作用 注:以鲫鱼池塘养殖水为基质,加标量为10 ng/L。 |
为有效消除基质效应的影响,采用同位素稀释方法进行定量。这是由于同位素内标物与待测物的结构和理化性质最为相似,受到基质干扰效应类似,因而能够有效抵消样品在离子化时的基质效应[27]。采用公式(1)来评价23种镇静剂在不同基质中的基质效应(ME)[28]:
| $ \mathrm{ME}=\left(\frac{\text { 基质匹配标准曲线的斜率 }}{\text { 溶剂标准曲线的斜率 }} 1\right) \times 100 \% $ | (1) |
式中:基质匹配标准曲线的斜率——空白基质配制标准溶液制得的工作曲线的斜率;溶剂标准曲线的斜率——纯溶剂配制的标准溶液制得的工作曲线的斜率。
当ME值>0时,表示存在基质增强效应;当ME值<0时,表示存在基质抑制效应。通常当ME绝对值>20%时,表明基质效应较大,应采取适当措施来降低基质效应。
外标法与内标法测定23种镇静剂时的基质效应见图 3。由图 3可见,用外标法时,23种镇静剂在池塘养殖水体中除氯安定、去甲基氯硝西泮、乙酰丙嗪、阿扎哌隆的ME值>20%外,其余镇静剂的ME值均未超过20%,这可能由于池塘养殖水体中富含各种生物体及它们的排泄物等,成分复杂,干扰较多,严重影响目标化合物的离子化。采用内标法时,23种镇静剂在池塘养殖水中的ME值均<20%,有效抑制了基质效应。因此选用内标法可抑制基质效应,确保结果的可靠性。

|
图 3 外标法与内标法测定23种镇静剂时的基质效应 |
用空白养殖水样品基质逐级稀释配制不同质量浓度的混合标准工作溶液。在1.2节的分析条件下,以各化合物的质量浓度(x,μg/L)为横坐标,以峰面积与对应内标的峰面积比值为纵坐标(y),得到各化合物的标准曲线。根据取样量,以3和10倍信噪比确定检出限(LOD)和定量限(LOQ)。结果表明,23种镇静剂在0.5~100 ng/L范围内线性关系良好,相关系数(r)均≥0.99,结果见表 2。由表 2可见,23种镇静剂的最低检出限为0.1~0.3 ng/L,最低定量限为0.4~1.0 ng/L,本方法对养殖水体中23种镇静剂的检测灵敏度较高。
| 表 2 23种镇静剂的线性方程、相关系数、检出限和定量限 |
本方法采用加标回收实验进行准确度和精密度评价。选取3种典型不含待测物的池塘养殖水作为空白基质,分别添加质量浓度为2.0,20,100 ng/L的23种镇静剂溶液,按照1.2.2节前处理方法进行处理后上机分析,每个质量浓度水平平行测定6次,计算各化合物的加标回收率和相对标准偏差(RSD),结果见表 3。由表 3可见,23种镇静剂的加标回收率为73.5%~117.6%,RSD为1.1%~9.9%(均<15%)。可见本方法的准确度和精密度均满足实验室检测要求。
| 表 3 23种镇静剂的加标回收率和精密度(n=6) |
采用本方法对10份不同品种养殖水进行定量分析,其中1份鲫鱼养殖水中检测出3 ng/L的地西泮,1份中华绒螯蟹养殖水中检测出5 ng/L的地西泮和7 ng/L的氯丙嗪。
3 结语建立了同时检测养殖水体中23种镇静剂的LC-MS/MS分析方法,该方法通过Oasis HLB柱富集净化,利用同位素稀释和基质标准曲线,有效降低了基质效应。通过方法学验证和实际样品的检测,23种镇静剂在0.5~100 ng/L质量浓度范围内线性关系良好(r>0.99),检出限和定量限分别为0.1~0.3和0.4 ~1.0 ng/L,加标回收率为73.5%~117.6%,RSD为1.1%~9.9%。表明该方法前处理简单,能够实现多种化合物同时分离,大大缩短了检测时间,方法检出限低、精密度较好、准确度较高,适用于日常环境水中多种镇静剂类药物残留定性定量分析的需求。
| [1] |
ZHANG L Q, WU P G, JIN Q, et al. Multi-residue analysis of sedative drugs in human plasma by ultra-high performance liquid chromatography tandem mass spectrometry[J]. Journal of Chromatography B, 2017, 1072: 305-314. |
| [2] |
OCHOA J G, KILGO W A. The role of benzodiazepines in the treatment of epilepsy[J]. Current Treatment Options in Neurology, 2016, 18(4): 1-11. |
| [3] |
CHEN K, WU M, CHEN C, et al. Impacts of chronic exposure to sublethal diazepam on behavioral traits of female and male zebrafish(Danio rerio)[J]. Ecotoxicology and Environmental Safety, 2021, 208: 111747. DOI:10.1016/j.ecoenv.2020.111747 |
| [4] |
MOHAMMAD V, ZARRIN E. Magneticnanoparticle-reinforceddual-template molecuarly imprinted polymer for the simultaneous detemination of oxazepam and diazepam using an electorchemical approch[J]. Journal of Analytical Chemistry, 2022, 77(5): 625-639. DOI:10.1134/S1061934822050082 |
| [5] |
王守英, 孔聪, 杨光昕, 等. 上海市售水产品地西泮及去甲地西泮残留调查分析[J]. 农产品质量与安全, 2020(3): 31-35, 67. |
| [6] |
四川省监督管理局. 四川省市场监督管理局关于26批次食品不合格情况的通告(2020年第42号)[EB/OL]. (2020-10-09). http://scjgj.sc.gov.cn/scjgj/c104536/2020/10/9/bfd8dad519074e7280c49ba27298d402.shtml.
|
| [7] |
天津市市场监督管理委员会. 天津市蓟州区市场监督管理局2020年第7期食品安全监督抽检信息[EB/OL]. (2020-12-08). http://scjg.tj.gov.cn/tjsjzqscjdglj/xwdt_57928/gstg_57930/spcjxx_57932/202012/t20201208_4691851.html.
|
| [8] |
李晋成, 刘欢, 吴立冬, 等. 动物体内麻醉剂残留检测技术研究进展[J]. 食品科学, 2014, 35(5): 251-256. |
| [9] |
惠芸华, 蔡友琼, 于慧娟. 镇静类药物在活鱼运输中的应用研究进展[J]. 中国渔业质量与标准, 2014, 4(2): 39-43. |
| [10] |
BRODIN T, FICK J, JONSSON M, et al. Dilute concentrations of a psychiatric drug alter behavior of fish from natural populations[J]. Science, 2013, 339: 814-815. DOI:10.1126/science.1226850 |
| [11] |
李桂敏, 宁保安, 白家磊, 等. 地西泮单克隆抗体的制备及其酶联免疫吸附检测方法的建立[J]. 食品安全质量检测学报, 2014, 5(3): 956-963. |
| [12] |
邢丽梅, 谭家镒, 李发美, 等. 血、尿中氯硝西泮及其代谢物7-氨基氯硝西泮的GC-ECD法检测[J]. 分析试验室, 2003, 22(1): 28-31. |
| [13] |
王占良, 张建丽, 张亦农. 气相色谱-质谱联用法检测保健品中8种安眠镇静类药物[J]. 质谱学报, 2009, 30(5): 282-286. |
| [14] |
MUSAVVIR A M, CARLY S, DANIEL R, et al. Pharmaceu-ticals in grocery market fish fillets by gas chromatography-mass spectrometry[J]. Food Chemistry, 2016, 190: 529-536. DOI:10.1016/j.foodchem.2015.06.003 |
| [15] |
BIANCA M C B, DAIANE C P A, ADELIR A S, et al. Residual determinationof anesthetic menthol in fishes by SDME/GC-MS[J]. Food Chemistry, 2017, 229: 674-679. DOI:10.1016/j.foodchem.2017.02.087 |
| [16] |
魏晋梅, 罗玉柱, 白云旭. 高效液相色谱法同时测定羊肉中11种镇静剂类药物[J]. 食品工业科技, 2014, 33(8): 252-255. |
| [17] |
LI P D, HAN H R, ZHAI X H, et al. Simultaneous HPLC-UV determination of ketamine, xylazine, and midazolam in canine plasma[J]. Journal of Chromatographic Science, 2012, 50(2): 108-113. DOI:10.1093/chromsci/bmr036 |
| [18] |
张烁, 周爽, 陈达炜, 等. 畜肉中10种镇静剂残留的超高效液相色谱-串联质谱测定方法[J]. 分析测试学报, 2014, 33(11): 1213-1218. |
| [19] |
STORHAUG L W, ENGER A, HJELMELAND J K, et al. Prolonged excretion of 7-aminoclonazepam in urine after repeated ingestion of clonazepam: A case report[J]. Forensic Science International, 2012, 222(1-3): 33-35. DOI:10.1016/j.forsciint.2012.04.031 |
| [20] |
孙雷, 张骊, 徐倩, 等. 超高效液相色谱-串联质谱法检测猪肉和猪肾中残留的10种镇静剂类药物[J]. 色谱, 2010, 28(1): 38-42. |
| [21] |
袁圣柳, 李晓锋, 姜晓满, 等. 自动固相萃取-高效液相色谱串联质谱法测定生活污水中13种抗精神病药物[J]. 分析化学, 2013, 41(1): 49-56. |
| [22] |
冯静, 邹淼, 陈曦, 等. 超高效液相色谱-串联质谱法检测牛肉中16种镇静剂类药物残留[J]. 食品安全质量检测学报, 2019, 10(10): 3091-3096. |
| [23] |
渠岩, 路勇, 冯楠, 等. 基质固相分散-超高效液相色谱-串联质谱法同时测定畜禽肉中残留的13种镇静药物[J]. 食品科学, 2012, 33(8): 252-255. |
| [24] |
张力群, 金铨, 刘少颖, 等. 超高效液相色谱-串联质谱法同时检测环境水中5种苯二氮卓类镇静剂药物[J]. 中国卫生检验杂志, 2018, 28(2): 142-145. |
| [25] |
张昕, 张晶, 邵兵. 固相萃取-超高效液相色谱-串联质谱法测定水中5种常用苯二氮卓类药物[J]. 中国食品卫生杂志, 2017, 29(6): 684-689. |
| [26] |
环境保护部. 水质采样技术指导: HJ 494—2009[S]. 北京: 中国环境科学出版社, 2009.
|
| [27] |
王立琦, 贺利民, 曾振灵, 等. 液相色谱-串联质谱检测兽药残留中的基质效应研究进展[J]. 质谱学报, 2011, 32(6): 321-332. |
| [28] |
杨洪生, 张秋云, 谭秀慧, 等. 同位素稀释-液相色谱-串联质谱法同时测定水产品中13种镇静剂残留[J]. 食品安全质量检测学报, 2021, 12(15): 6017-6025. |
 2024, Vol. 16
2024, Vol. 16 

