2. 广西壮族自治区生态环境监测中心,广西 南宁 530028;
3. 广西新污染物监测预警与环境健康评估重点实验室,广西 南宁 530028;
4. 南宁市核与辐射安全监督管理站,广西 南宁 530015
2. Guangxi Zhuang Autonomous Region Ecological and Environmental Monitoring Center, Nanning, Guangxi 530028, China;
3. Guangxi Key Laboratory of Emerging Contaminants Monitoring, Early Warning and Environmental Health Risk Assessment, Nanning, Guangxi 530028, China;
4. Nanning Nuclear and Radiation Safety Supervision and Administration Station, Nanning, Guangxi 530015, China
全氟和多氟烷基物质(PFASs)是近年来广受关注的一类新污染物。其脂肪烃碳链上氢原子全部或部分被氟原子取代,形成具有CnF2n+1基团的化合物[1-2]。根据C—F链长度可将PFASs分为短链PFASs和长链PFASs[3],长链PFASs指含≥7个全氟碳的全氟烷基羧酸(PFCAs)和含≥6个全氟碳的全氟烷基磺酸(PFSAs)[4]。由于其具有化学稳定性、抗腐蚀性和耐高温性等特点[5],被广泛应用于农药、表面防污处理剂[6]、消防灭火剂[7]和食品包装材料[8]等行业。目前,PFASs在土壤、沉积物、水体、空气以及野生动物甚至人类体液等多种介质中均有不同程度的检出[9]。在微生物中,PFASs磺酸类毒性高于羧酸类,碳链越长毒性越大[10]。长期接触PFASs会导致人类和动物内分泌紊乱和生殖畸形[11]。2009年,全氟辛烷磺酸(PFOS)和全氟辛烷磺酰氟(POSF)被列入《斯德哥尔摩公约》中的持久性有机污染物。2023年3月,我国将全氟己基磺酸及其盐类(PFHxS)、全氟辛酸(PFOA)和全氟辛基磺酸(PFOS)列入生态环境部重点管控新污染物清单,禁止生产、加工使用(除特殊用途)和进出口[12]。
有研究表明,污水处理厂的出水成为地表水中PFASs的主要来源之一[13]。中国东南沿海[14]、上海[15]、北京[16]、意大利[17]、美国[18]等多个国家和地区对污水处理厂中PFASs污染水平开展了研究。目前,广西省对于污水处理厂不同污水处理工艺中PFASs污染水平和去除效率的研究相对较少。现选择广西省2个城市的3家污水处理厂(P1、P2、P3)进行研究,以17种常见的PFASs作为目标污染物,研究它们在3种常见污水处理工艺中的来源和污染水平,比较不同处理工艺对这些目标污染物的去除率和对纳污河流生态系统的潜在风险,以期为广西新污染物溯源、管控提供数据支持和科学依据。
1 材料与方法 1.1 采样信息
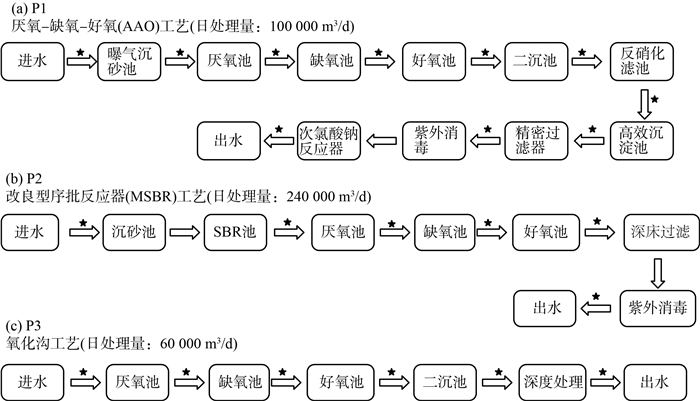
|
图 1 污水处理厂工艺流程及采样位置 注:“★”代表采样位置。 |
仪器:Oasis WAX固相萃取柱(6cc/150 mg,美国Waters公司);ACQUITY UPLC-XEVO TQ-XS超高效液相色谱质谱联用仪(美国Waters公司);ACQUITY UPLC Ⓒ BEH C18色谱分析柱(1.7 μm,2.1 mm×100 mm,美国Waters公司);GM-0.50隔膜真空泵(天津市腾达过滤器件厂);Supelco-12孔固相萃取装置(美国色谱科公司);0.45 μm玻璃纤维滤膜(海宁市创伟过滤设备器材厂);0.22 μm尼龙有机过滤头(天津市津腾实验设备有限公司);5 mL一次性注射管(广西北仓河医科工业集团有限公司)。
试剂:含有17种PFASs的混合标准品(100 g/L),标液中含有全氟丁烷(PFBA,98%)、全氟戊酸(PFPeA,98%)、全氟己酸(PFHxA,98%)、全氟庚酸(PFHpA,98%)、全氟辛酸(PFOA,96%)、全氟壬酸(PFNA,96.3%)、全氟癸酸(PFDA,98%)、全氟十一烷酸(PFUnDA,97.3%)、全氟十二烷酸(PFDoDA,93.2%)、全氟十三烷酸(PFTrDA,98%)、全氟十四烷酸(PFTeDA,96%)、全氟十六烷酸(PFHxDA,95.3%)、全氟十八烷酸(PFODA,96%)、全氟丁烷(PFBS,98%)、全氟己基磺酸(PFHxS,98.6%)、全氟辛基磺酸(PFOS,89.8%)、全氟癸烷磺酸(PFDS,95%),均购自Fisrt standard公司(中国);HPLC Grade乙腈(ACN,>99.7%)、甲醇(99.9%),均购自Fisher公司(美国)。
1.3 样品采集与预处理使用预先洗涤干净并干燥的不锈钢材质的采样器和500 mL棕色聚丙烯样品瓶采集水样。所有样品均在0~4 ℃避光保存,30 d内完成分析工作。
使用隔膜真空泵将水样通过0.45 μm玻璃纤维滤膜进行过滤,然后使用12孔固相萃取装置将水样通过Oasis WAX柱进行固相萃取。萃取前依次使用4 mL的2%氨水-甲醇、甲醇和超纯水活化Oasis WAX柱,活化过程保持填料层湿润。将样品通过Oasis WAX柱,流速控制在约1滴/s。萃取结束后,使用4 mL的25 mmol/L醋酸铵水溶液进行淋洗,弃去淋洗液。真空冷冻干燥后,依次使用4 mL的甲醇和2%氨水-甲醇进行淋洗,收集淋洗液至10 mL氮吹管中,氮吹浓缩至1 mL,使用5 mL注射器将浓缩的样品通过0.22 μm尼龙滤膜至2 mL的棕色上样小瓶中,0~4 ℃保存。
1.4 分析条件 1.4.1 色谱条件流动相A:2 mmol/L醋酸铵水溶液;流动相B:乙腈。运行时间:20 min;液体流速:0.3 mL/min;色谱柱温:40 ℃;进样量:5 μL。色谱流动洗脱按照梯度洗脱程序进行。
1.4.2 质谱条件离子源:电喷雾离子源(ESI),负离子模式;监测方式:多反应监测(MRM);气帘气压力:241.3 kPa;喷雾电压:-4 500 V;雾化温度:550 ℃;雾化气压力:379.2 kPa;铺助气压力:413.7 kPa。
1.5 质量控制与质量保证17种PFASs采用外标法进行定量分析,以甲醇作为溶剂逐级稀释PFASs标液制备成1.0~100.0 μg/L的PFASs标准使用溶液,经超高效液相色谱串联质谱(UPLC-MS-MS)分析获得标准曲线。17种PFASs的方法检出限及加标回收率见表 1。由表 1可见,标准曲线的决定系数(R2)均≥0.995。方法检出限为0.1~0.4 ng/L,加标回收率为55.0%~116%。质控措施包括全程序空白、实验室空白、平行双样。空白样品均无PFASs检出,平行样检测结果平均相对标准偏差≤10%。
| 表 1 17种PFASs的方法检出限及加标回收率 |
以3种营养级的生物物种(藻类、水蚤和鱼类)作为保护对象,分析PFASs对水生生物的毒性。按照风险商(RQ)的计算公式,计算12种PFASs对淡水环境中藻类、水蚤和鱼类的RQ值,评估PFASs对水生环境的生态风险。根据RQ值将风险水平划分为3类:RQ<0.1,低风险;0.1<RQ<1,中风险;RQ>1,高风险[19-20]。
| $ \mathrm{RQ}=\frac{\mathrm{MEC}}{\mathrm{PNEC}} $ | (1) |
| $ \mathrm{PNEC}=\frac{\mathrm{LC}_{50}}{\mathrm{AF}}=\frac{\mathrm{EC}_{50}}{\mathrm{AF}} $ | (2) |
式中:MEC——环境中测得污染物的质量浓度,ng/L;EC50——半数效应质量浓度,ng/L;LC50——半数致死质量浓度,ng/L;AF——评估系数;PNEC——预测无效应质量浓度,ng/L。
2 结果与讨论 2.1 污水处理厂进、出水中PFASs的污染特征和来源分析3个污水处理厂进、出水中PFASs的组成和质量浓度见图 2。
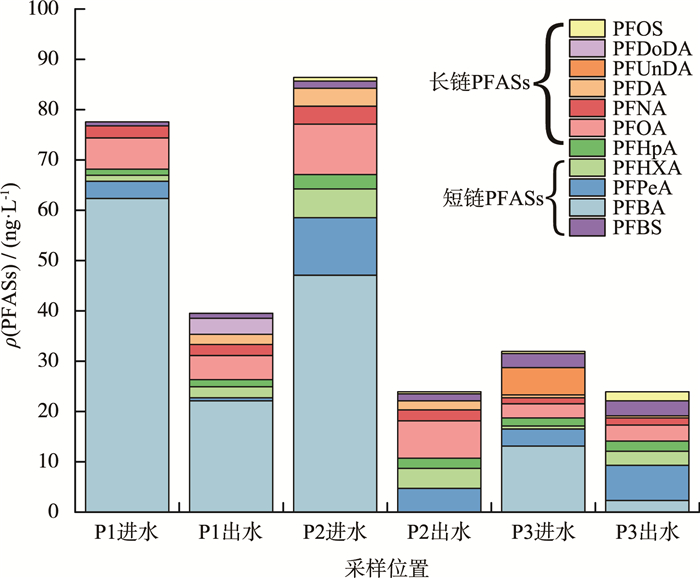
|
图 2 3个污水处理厂进、出水中PFASs的组成和质量浓度 |
由图 2可见,在进水中,不同PFASs组分检出率为33.3%~100%,短链PFASs和长链PFASs的平均检出率分别为100%和67%,污染水平呈现短链PFASs>长链PFASs的特征。进水中PFASs质量浓度为32.0~86.4 ng/L,主要污染物为PFBA、PFPeA和PFOA,贡献率分别为58.7%,9.4%和9.4%。与罗马尼亚(376~527 ng/L)[21]、墨西哥(419~591 ng/L)[22]2个国家,以及与陕西(1.5~62.5 ng/L)[13]、深圳(14~67 ng/L)[23]污水处理厂进水中的PFASs质量浓度相比,本研究的3个污水处理厂进水中的PFASs质量浓度处于中等水平。出水中PFASs质量浓度为24.0~39.6 ng/L,低于我国《生活饮用水卫生标准》(GB 5749—2022)[24]对PFASs的规定。出水的PFASs质量浓度低于进水,表明污水处理过程对PFASs具有一定的去除作用。出水与进水具有相同的污染特征,PFBA、PFOA、PFPeA为出水的主要污染物,贡献率分别为22%,18.8%和16.9%。相较于进水,PFBA贡献率下降,PFOA和PFPeA贡献率上升。污水处理过程对PFASs的去除可能存在以下几个方面:一部分PFASs通过生物处理过程转化为稳定产物[25],一部分转移至污泥[26],另一部分通过出水排放至纳污河流[13]。近年来,短链PFASs逐渐取代具有更高生物富集性和毒性的长链PFASs,在工业上广泛应用,这也是短链PFASs在环境中的污染水平高于长链PFASs的主要原因[27],这与本研究的结果一致。
对3个污水处理厂的进水来源进行调查,P1和P3的进水主要由生活污水构成,P2进水中含有部分工业废水。因此,P1和P3进水中的PFASs可能主要来源于生活污水中的含氟消费品[21],如防水材料、纺织品等产品在洗涤过程释放的多氟超细纤维[28],以及化妆品、食品包装、清洗剂[29]和杀虫剂[6]等。P3相较于P1,进水中PFASs的质量浓度较低。可能由于P1来水收集区域的人口数量是P3的2.5倍,人口较多的城市使用和消费含氟消费品也随之增加,这与文献[30]的研究结果相符。PFASs被广泛应用于金属加工[31]、纺织工业[32]、食品包装、电子、化工生产[33]等行业。P2进水来源组成见图 3。由图 3可见,PFASs不仅来源于生活污水,还来源于包括金属加工、化学制造、电子加工等生产过程产生的工业废水。
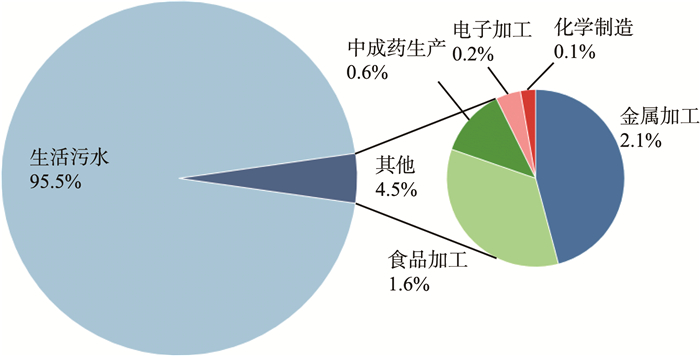
|
图 3 P2进水来源组成 |
AAO工艺各单元PFASs的组成及质量浓度见图 4。由图 4可见,各污水处理单元的PFASs总体组成与进水保持一致,但质量浓度存在差异。在生物处理阶段(厌氧池、缺氧池和好氧池),PFASs的去除率为51.5%,其中PFBA的去除率为73.5%,是该过程主要去除的物质。在深度处理阶段(二沉池、反硝化滤池、高效沉淀池和精密过滤器),反硝化滤池采用纳米有机生物滤料作为反应区,滤料的多孔结构可使污水中的PFASs附着在其中,对PFASs的去除率为28.7%。二沉池与精密过滤器中出现PF ASs质量浓度上升的情况,这可能是由于附着在污泥和过滤膜上的PFASs重新释放到水体中。深度消毒阶段,污水中的PFASs质量浓度从60.2 ng/L下降至39.6 ng/L,去除率为34.2%。说明该过程可以通过强氧化还原反应以及物理作用完全去除一部分PFASs(PFPeA、PFDoDA和PFUnDA)。这与文献[34]的研究相符,高级氧化和还原工艺可以将某种PFASs彻底从污水中去除。各污水处理阶段对PFASs的去除率排序为:生物处理阶段>深度消毒阶段>深度处理阶段。
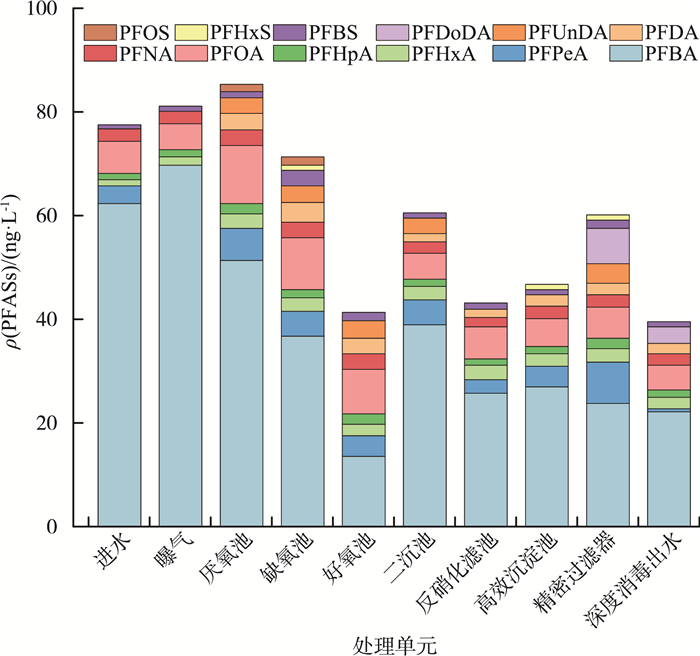
|
图 4 AAO工艺各单元PFASs的组成及质量浓度 |
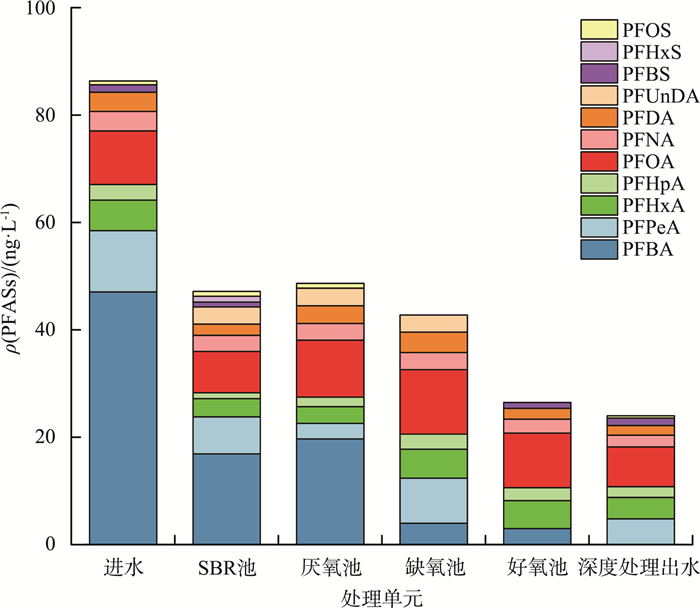
MSBR工艺各单元PFASs的组成和质量浓度见图 5。由图 5可见,污水经过SBR池后,PFASs质量浓度从86.4 ng/L下降至47.1 ng/L,去除率为45.5%。长链PFASs和短链PFASs的去除率分别为13.9%和56.4%,短链PFASs的去除效果优于长链PFASs。这可能由于在SBR池中发生了污泥吸附作用[34],使污水中PFASs质量浓度降低。经过生物处理阶段(厌氧池、缺氧池和好氧池),PFASs质量浓度从48.6 ng/L下降至26.5 ng/L,去除率为45.5%。短链PFASs和长链PFASs的去除率分别为63.8%和25.2%。好氧池是对PFASs去除率贡献最高的生物处理单元,短链PFASs和长链PFASs的去除率分别为55.5%和31.3%。在深度处理阶段,PFASs去除率为9.43%。各污水处理阶段对PFASs的去除率排序为:SBR池>生物处理阶段>深度处理阶段。
|
图 5 MSBR工艺各单元PFASs的组成和质量浓度 |
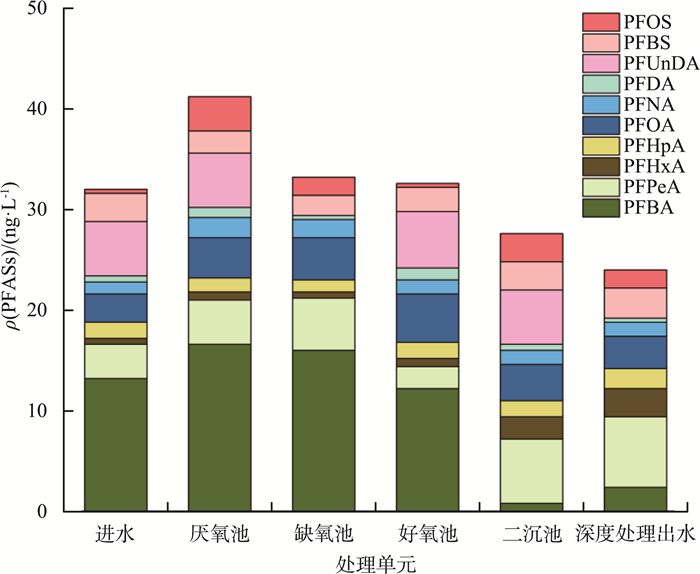
氧化沟工艺各单元PFASs的组成和质量浓度见图 6。
|
图 6 氧化沟工艺各单元PFASs的组成和质量浓度 |
由图 6可见,厌氧池、缺氧池和好氧池污水的PFASs质量浓度分别为41.2,33.2和32.6 ng/L,生物处理阶段(厌氧池、缺氧池和好氧池)对PFASs的去除率为20.9%。在二沉池中,PFASs质量浓度从32.6 ng/L降至27.6 ng/L,去除率为15.3%。其中对PFBA的去除效果相对较好,去除率可达93.4%。在深度处理阶段,对PFASs的去除率为13.0%。氧化沟工艺对PFASs的去除率相对较低,不同的PFASs浓度会影响污泥的吸附效率[35],较低的PFASs浓度不利于污泥对其进行吸附。各污水处理阶段对PFASs的去除效率为:生物处理阶段>二沉池>深度处理阶段。
2.3 不同污水处理工艺对PFASs的去除率AAO、MSBR和氧化沟工艺对PFASs的去除效率见表 2。
| 表 2 AAO、MSBR和氧化沟工艺对PFASs的去除效率 |
由表 2可见,3种工艺在污水处理过程中对PFASs均呈现正去除现象,总体去除率排序为:MSBR(72.2%)>AAO(49.0%)>氧化沟(25.0%)。不同工艺对PFASs的去除率存在差异,可能与进水中PFASs浓度和污泥的吸附性能有关。进水中较高浓度的PFASs有利于吸附平衡正向移动,从而可以提高污泥对PFASs的吸附效率。污泥吸附性能可能会被由微生物所组成的菌胶团的数量影响,菌胶团具有很强的吸附能力,可以有效吸附和分解有机物[36]。有研究指出,微生物胞体中的蛋白质有助于污泥吸附PFASs[37],同时胞体可以通过附着到污泥表面来改变污泥的吸附性质并提供更多的吸附点位[38]。因此不同工艺的微生物浓度不同,对污泥产生的作用也存在差异,从而导致对PFASs的去除效率存在差异。不同处理工艺中优势微生物种类不同,导致PFASs的生物降解效率不同[15]。污水中的总有机碳(TOC)对污泥吸附PFASs也具有不同程度的影响,碳链>5的PFASs,TOC与其吸附能力之间的相关性强于碳链<5的PFASs[37]。水力停留时间(HRT)也会影响PFASs的去除效果,适当地延长HRT,可使PFASs与污泥充分接触,从而吸附平衡正向移动[39]。
短链PFASs的去除率排序为:MSBR>AAO>氧化沟,对短链PFASs去除效果较好的处理单元为SBR池和好氧池。长链PFASs的去除率排序为:MSBR>氧化沟>AAO,去除率均低于短链PFASs。不同种类PFASs的去除率存在差异,这可能与PFASs的物理和化学性质有关,包括PFASs的碳链长度、碳链组成和官能团[13]。有研究指出,随着碳链长度的增加,PFASs与固相之间的疏水作用增强,而静电相互作用逐渐减弱[40]。短链PFASs在吸附过程中通过静电作用和孔隙堵塞与污泥发生相互作用,长链PFASs更容易受到疏水作用的主导[41]。根据本研究的污水处理厂对PFASs的去除效果,在污泥吸附过程中对PFASs产生的静电作用可能大于疏水作用。氢取代、醚键的插入和酸基等官能团通过影响分子性质,从而影响PFASs的去除效果,如相同碳链长度的PFSAs疏水性高于PFCAs,疏水性越强越容易被污泥所吸附[42]。同时官能团的位置和数量以及不饱和的位置和程度也会影响微生物对PFASs的降解和转化作用[43]。此外,负去除现象可能与二级处理过程中的回流污泥有关,导致已经吸附饱和的污泥重新释放部分PFASs到污水中[44],可能也存在前驱体的转化[45]。
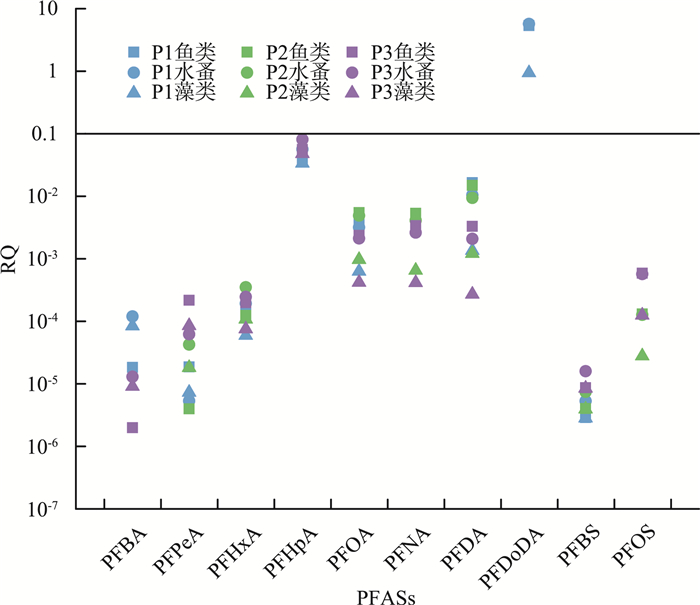
2.4 生态风险评价 2.4.1 生态风险评价结果针对污水处理厂出水中检出的PFASs组分,对鱼类、水蚤以及藻类3种淡水生物进行生态风险分析。基于LC50、EC50以及AF值[3, 46-48],计算纳污河流的生态风险。PFASs对纳污河流中鱼类、水蚤以及藻类产生的RQ值见图 7。
|
图 7 PFASs对纳污河流中鱼类、水蚤以及藻类产生的RQ值 |
由图 7可见,P1出水中的PFDoDA对纳污河流中的鱼类和水蚤构成了高生态风险,对藻类构成中等生态风险。P2和P3出水中的PFASs对3种水生生物产生的RQ值均<0.1,因此对纳污河流产生的生态风险较低。与其他河流相比,如长江中游[49]、华南龙岗区流域[50]以及辽河流域[51]等,PFASs对3个污水处理厂的纳污河流产生的生态风险较低。短链PFASs对藻类和水蚤构成更高的生态风险,长链PFASs对3种水生生物产生的RQ值均<0.1,PFASs对鱼类构成的生态风险高于藻类和水蚤,可能会诱发鱼类的生殖障碍[52]。因此,对短链和长链PFASs产生的生态风险都应该引起重视,可对相关流域进行追踪溯源,形成源头禁限、过程减排、末端治理的全过程环境风险管控措施。
2.4.2 不确定性分析在采样和实验阶段,不确定性主要来源于单次采样的不完全性以及PFASs组分和污水处理厂分析数量较少的数据不全面性。季节、温度和降水量等自然因素具有不确定性,由于条件限制,本实验只进行了一次采样分析,研究结果只能说明一个时期研究区域的生态风险。有条件时,应根据丰水期、平水期、枯水期和四季分别进行采样分析,更完整深入地分析研究区域中PFASs的污染特征和评价其生态风险。目前,PFASs在生产生活上使用的组分越来越丰富,更多的PFASs组分进入环境中。本研究仅分析了3个污水处理厂中17种PFASs,分析数据较为局限,不能完整地分析研究区域的生态风险,需要进一步增加PFASs组分和排入相同河流的污水处理厂的采样数量。此外,风险商法被广泛应用于生态风险评价,但也存在一定的局限性。该法虽然能够给出纳污河流中PFASs组分的RQ值,但是只能粗略判断PFASs组分对纳污河流是否造成危害,不能将其作为生态评价的唯一标准。该法只能分析单一组分对河流造成的生态风险,对多组分的协同作用造成生态风险分析评价存在不足。因此,在今后的生态风险评价工作中应采用多种评价分析方法进行综合评价,以获取更准确的评价结果。
3 结论(1) 选择广西省3家污水处理厂(P1、P2、P3),对17种PFASs进行研究。结果表明,进、出水中检测出12种PFASs,检出率为33.3%~100%。进水中PFASs质量浓度为32.0~86.4 ng/L。污染水平呈现短链PFASs>长链PFASs的特点,PFBA、PFPeA和PFOA是污水中的主要污染物。
(2) 3种污水处理工艺对PFASs的去除率为:MSBR>AAO>氧化沟,去除率呈现短链PFASs>长链PFASs的特点。
(3) P1出水中的PFDoDA对纳污河流中的鱼类和水蚤构成了高生态风险,对藻类构成中等生态风险。P2和P3出水中的PFASs对3种水生生物产生的RQ值均<0.1,对纳污河流构成的生态风险较低。
| [1] |
杨觅, 赵璇, 黄馨仪, 等. 超高效液相色谱-串联三重四极杆质谱法检测血清中12种全氟化合物[J]. 现代预防医学, 2022, 49(10): 1867-1873, 1911. |
| [2] |
刘勋涛, 李春阳, 陈汐昂, 等. 全氟化合物控制政策、识别控制技术及生态风险评估进展[J]. 农业环境科学学报, 2023, 42(9): 1911-1927. |
| [3] |
JIANG W, MUHAMMAD J, ZHIFEN W, et al. Spatiotemporal distribution, sources and ecological risks of perfluorinated compounds(PFCs) in the Guanlan River from the rapidly urbanizing areas of Shenzhen, China[J]. Chemosphere, 2020, 245: 125637. DOI:10.1016/j.chemosphere.2019.125637 |
| [4] |
COUSINS I T, DEWITT J C, GLVGE J, et al. Strategies for grouping per-and polyfluoroalkyl substances(PFAS) to protect human and environmental health[J]. Environmental Science: Processes & Impacts, 2020, 22(7): 1444-1460. |
| [5] |
张美, 楼巧婷, 邵倩文, 等. 全氟化合物污染现状及风险评估的研究进展[J]. 生态毒理学报, 2019, 14(3): 30-53. |
| [6] |
朱冰春, 许天明, 孔小林, 等. 全氟异丙基苯衍生物的合成及其在新农药创制中的应用[J]. 农药, 2009, 48(10): 712-714. |
| [7] |
何宗健, 甘甜, 彭希珑, 等. 环鄱阳湖城市污水处理厂污泥中全氟化合物的污染特征[J]. 南昌大学学报(工科版), 2020, 42(2): 103-108. |
| [8] |
OLGA S A, ATHANASIOS S S. Review on the occurrence, fate and removal of perfluorinated compounds during wastewater treatment[J]. Science of The Total Environment, 2015, 524-525: 81-92. DOI:10.1016/j.scitotenv.2015.04.023 |
| [9] |
LIU Y, MA L, YANG Q, et al. Occurrence and spatial distribution of perfluorinated compounds in groundwater receiving reclaimed water through river bank infiltration[J]. Chemosphere, 2018, 211: 1203-1211. DOI:10.1016/j.chemosphere.2018.08.028 |
| [10] |
CAI Y, CHEN H, YUAN R, et al. Toxicity of perfluorinated compounds to soil microbial activity: Effect of carbon chain length, functional group and soil properties[J]. Science of The Total Environment, 2019, 690: 1162-1169. DOI:10.1016/j.scitotenv.2019.06.440 |
| [11] |
RODRIGUEZ-VARELA M, DURAN-ALVAREZ J C, JIMENEZ-CISNEROS B, et al. Occurrence of perfluorinated carboxylic acids in Mexico City's wastewater: A monitoring study in the sewerage and a mega wastewater treatment plant[J]. Science of The Total Environment, 2021, 774: 145060. DOI:10.1016/j.scitotenv.2021.145060 |
| [12] |
中华人民共和国生态环境部. 重点管控新污染物清单(2023年版)[EB/OL]. (2022-12-30)[2023-11-12]. https://www.mee.gov.cn/xxgk2018/xxgk/xxgk02/202212/t20221230_1009167.html.
|
| [13] |
WENBIN C, FANG Y, EN H, et al. Occurrence, fate and risk assessment of per-and polyfluoroalkyl substances in wastewater treatment plants in Shaanxi, China[J]. Environmental Pollution, 2022, 314: 120226. DOI:10.1016/j.envpol.2022.120226 |
| [14] |
CHUNJIE G, CHENYE X, QUAN Z, et al. Congener-and isomer-specific perfluorinated compounds in textile wastewater from Southeast China[J]. Journal of Cleaner Production, 2021, 320: 128897. DOI:10.1016/j.jclepro.2021.128897 |
| [15] |
ZHANG C, YAN H, LI F, et al. Occurrence and fate of perfluorinated acids in two wastewater treatment plants in Shanghai, China[J]. Environmental Science and Pollution Research, 2015, 22(3): 1804-1811. DOI:10.1007/s11356-013-2044-8 |
| [16] |
潘媛媛, 史亚利, 王杰明, 等. 北京市污水处理厂中全氟化合物的污染水平[J]. 中国科学: 化学, 2011, 41(6): 1095. |
| [17] |
SARA C, SARA V, STEFANO P, et al. Sources and fate of perfluorinated compounds in the aqueous environment and in drinking water of a highly urbanized and industrialized area in Italy[J]. Journal of Hazardous Materials, 2015, 282: 51-60. DOI:10.1016/j.jhazmat.2014.06.007 |
| [18] |
CHARLES E S, JENNIFER L H, LAUREL E S, et al. Occurrence of quantifiable and semi-quantifiable poly-and perfluoroalkyl substances in united states wastewater treatment plants[J]. Water Research, 2023, 233: 119724. DOI:10.1016/j.watres.2023.119724 |
| [19] |
SUN R, WU M, TANG L, et al. Perfluorinated compounds in surface waters of Shanghai, China: Source analysis and risk assessment[J]. Ecotoxicology and Environmental Safety, 2018, 149: 88-95. DOI:10.1016/j.ecoenv.2017.11.012 |
| [20] |
GREDELJ A, BARAUSSE A, GRECHI L, et al. Deriving predicted no-effect concentrations(PNECs) for emerging contaminants in the river Po, Italy, using three approaches: Assessment factor, species sensitivity distribution and AQUATOX ecosystem modelling[J]. Environment International, 2018, 119: 66-78. DOI:10.1016/j.envint.2018.06.017 |
| [21] |
CHIRIAC F L, PIRVU F, PAUN I, et al. Perfluoroalkyl substances in Romanian wastewater treatment plants: Transfer to surface waters, environmental and human risk assessment[J]. Science of The Total Environment, 2023, 164576. |
| [22] |
MARIO R V, JUAN C D Á, BLANCA J C, et al. Occurrence of perfluorinated carboxylic acids in Mexico City's wastewater: A monitoring study in the sewerage and a mega wastewater treatment plant[J]. Science of The Total Environment, 2021, 774: 145060. DOI:10.1016/j.scitotenv.2021.145060 |
| [23] |
WANG X, ZHANG R, ZHANG H, et al. Impact of biological treatment techniques on perfluoroalkyl acids emissions in municipal sewage[J]. Water, Air, & Soil Pollution, 2016, 227(5): 149. |
| [24] |
国家市场监督管理总局, 国家标准化管理委员会. 生活饮用水卫生标准: GB 5749—2022[S]. 北京: 中国标准出版社, 2022.
|
| [25] |
SHU Z, XIAOXIA L, NING W, et al. Biotransformation potential of 6:2 fluorotelomer sulfonate(6:2 FTSA) in aerobic and anaerobic sediment[J]. Chemosphere, 2016, 154: 224-230. DOI:10.1016/j.chemosphere.2016.03.062 |
| [26] |
OLGA S A, HENRIK R A, NIKOLAOS S T, et al. Sorption of perfluorinated compounds onto different types of sewage sludge and assessment of its importance during wastewater treatment[J]. Chemosphere, 2014, 111: 405-411. DOI:10.1016/j.chemosphere.2014.03.087 |
| [27] |
张慧, 王世亮, 余杨. 乐安河河流水体典型全氟化合物的浓度及其前体物的污染贡献[J]. 环境科学, 2020, 41(7): 3204-3211. DOI:10.3969/j.issn.1000-6923.2020.07.049 |
| [28] |
SCHELLENBERGER S, JÖNSSON C, MELLIN P, et al. Release of side-chain fluorinated polymer-containing microplastic fibers from functional textiles during washing and first estimates of perfluoroalkyl acid emissions[J]. Environmental Science & Technology, 2019, 53(24): 14329-14338. |
| [29] |
ULRIKA E, PETER H, ANNA K. Contribution of precursor compounds to the release of per-and polyfluoroalkyl substances(PFASs) from waste water treatment plants(WWTPs)[J]. Journal of Environmental Sciences, 2017, 61: 80-90. DOI:10.1016/j.jes.2017.05.004 |
| [30] |
PIAO H T, JIAO X C, GAI N, et al. Perfluoroalkyl substances in waters along the Grand Canal, China[J]. Chemosphere, 2017, 179: 387-394. DOI:10.1016/j.chemosphere.2017.03.133 |
| [31] |
ULRICH H, FREIER K P, GIERIG M. Getting on with persistent pollutants: Decreasing trends of perfluoroalkyl acids(PFAAs) in sewage sludge[J]. Chemosphere, 2016, 161: 527-535. DOI:10.1016/j.chemosphere.2016.07.048 |
| [32] |
GU C, XU C, ZHOU Q, et al. Congener-and isomer-specific perfluorinated compounds in textile wastewater from Southeast China[J]. Journal of Cleaner Production, 2021, 320: 128897. DOI:10.1016/j.jclepro.2021.128897 |
| [33] |
MU H, LI J, CHEN L, et al. Distribution, source and ecological risk of per-and polyfluoroalkyl substances in Chinese municipal wastewater treatment plants[J]. Environment International, 2022, 167: 107447. DOI:10.1016/j.envint.2022.107447 |
| [34] |
张春晖, 刘育, 唐佳伟, 等. 典型工业废水中全氟化合物处理技术研究进展[J]. 中国环境科学, 2021, 41(3): 1109-1118. DOI:10.3969/j.issn.1000-6923.2021.03.013 |
| [35] |
王凯, 郭昌胜, 张远, 等. 不同微生物处理工艺对全氟化合物的去除效果[J]. 环境科学研究, 2015, 28(1): 110-116. |
| [36] |
王国惠编. 环境工程微生物学——污染生物控制原理[M]. 2版. 北京: 科学出版社, 2020.
|
| [37] |
CHAO J Z, HONG Y, FEI L, et al. Sorption of short-and long-chain perfluoroalkyl surfactants on sewage sludges[J]. Journal of Hazardous Materials, 2013, 260: 689-699. DOI:10.1016/j.jhazmat.2013.06.022 |
| [38] |
MUSTAFA E E, HALE O, YU T, et al. Applicability of dynamic membrane technology in anaerobic membrane bioreactors[J]. Water Research, 2014, 48: 420-429. DOI:10.1016/j.watres.2013.09.054 |
| [39] |
PAN C G, LIU Y S, YING G G. Perfluoroalkyl substances(PFASs) in wastewater treatment plants and drinking water treatment plants: Removal efficiency and exposure risk[J]. Water Research, 2016, 106: 562-570. DOI:10.1016/j.watres.2016.10.045 |
| [40] |
LIN Y L, BAOLIN L, BIMI Z, et al. A systematic review on distribution, sources and sorption of perfluoroalkyl acids(PFAAs) in soil and their plant uptake[J]. Environmental Research, 2023, 231: 116156. DOI:10.1016/j.envres.2023.116156 |
| [41] |
SWADHINA P L, MELANIE K, LOKESH P P. A review of the occurrence, transformation, and removal of poly-and perfluoroalkyl substances(PFAS) in wastewater treatment plants[J]. Water Research, 2021, 199: 117187. DOI:10.1016/j.watres.2021.117187 |
| [42] |
JIANG L, YAO J, REN G, et al. Comprehensive profiles of per-and polyfluoroalkyl substances in Chinese and African municipal wastewater treatment plants: New implications for removal efficiency[J]. Science of The Total Environment, 2023, 857: 159638. DOI:10.1016/j.scitotenv.2022.159638 |
| [43] |
ASHENAFI B, ISHMAEL M, JI T, et al. A review of microbial degradation of per-and polyfluoroalkyl substances(PFAS): Biotransformation routes and enzymes[J]. Science of The Total Environment, 2023, 859: 160010. DOI:10.1016/j.scitotenv.2022.160010 |
| [44] |
汪磊, 张彰, 张宪忠, 等. 污水处理厂中全氟化合物的污染研究[J]. 环境科学学报, 2011, 31(7): 1363-1368. |
| [45] |
张悦清, 赵娅新, 余佳, 等. 城市水环境PFAAs前驱体污染特征及健康风险[J]. 中国环境科学, 2022, 42(12): 5896-5904. DOI:10.3969/j.issn.1000-6923.2022.12.047 |
| [46] |
JIE L, YU F A, JINGRUN H, et al. Polyfluoroalkyl substances in Danjiangkou Reservoir, China: Occurrence, composition, and source appointment[J]. Science of The Total Environment, 2020, 725: 138352. DOI:10.1016/j.scitotenv.2020.138352 |
| [47] |
JIE L, YUE G, NAN X, et al. Perfluoroalkyl substances in the Yangtze River: Changing exposure and its implications after operation of the Three Gorges Dam[J]. Water Research, 2020, 182: 115933. DOI:10.1016/j.watres.2020.115933 |
| [48] |
SARA V, DANIELA C, RICCARDO C, et al. Deriving environmental quality standards for perfluorooctanoic acid(PFOA) and related short chain perfluorinated alkyl acids[J]. Journal of Hazardous Materials, 2017, 323: 84-98. DOI:10.1016/j.jhazmat.2016.04.055 |
| [49] |
LENG Y, XIAO H, LI Z, et al. Occurrence and ecotoxicological risk assessment of perfluoroalkyl substances in water of lakes along the middle reach of Yangtze River, China[J]. Science of The Total Environment, 2021, 788: 147765. DOI:10.1016/j.scitotenv.2021.147765 |
| [50] |
HUANG C, ZHANG J, HU G, et al. Characterization of the distribution, source, and potential ecological risk of perfluorinated alkyl substances(PFASs) in the inland river basin of Longgang District, South China[J]. Environmental Pollution, 2021, 287: 117642. DOI:10.1016/j.envpol.2021.117642 |
| [51] |
汤家喜, 朱永乐, 李玉, 等. 辽河流域及周边水体中全氟化合物的污染状况及生态风险评价[J]. 生态环境学报, 2021, 30(7): 1447-1454. |
| [52] |
RIAZ R, JUNAID M, REHMAN M Y A, et al. Spatial distribution, compositional profile, sources, ecological and human health risks of legacy and emerging per-and polyfluoroalkyl substances(PFASs) in freshwater reservoirs of Punjab, Pakistan[J]. Science of The Total Environment, 2023, 856: 159144. DOI:10.1016/j.scitotenv.2022.159144 |
 2024, Vol. 16
2024, Vol. 16 

