全氟及多氟烷基化合物(PFAS) 是一类以碳链上氢原子被完全或部分替换为氟原子为特征的有机化学物质,因其含有极其稳定的C—F键,表现出极高的耐热、耐光和化学惰性[1-2]。自20世纪40年代以来,PFAS被广泛应用于众多工业领域,包括纺织、皮革、消防产品、电子产品、食品包装和不粘锅涂层等[3-7]。PFAS表现出显著的持久性和生物累积性[1],在生物体内的积累程度远超一些难降解的有机污染物,如有机氯农药和二噁英[8]。科学研究显示,暴露于特定浓度的PFAS中可能会对人类及其他生物体的健康造成不利影响[9-11]。PFAS在环境中的流动性及其在自然条件下难降解,导致它们可能在土壤中积累,对生态系统构成长期威胁[12-14]。因此,开发一种简便、灵敏和精准的分析方法,用于测定土壤中典型PFAS及其新型含氟替代物,对评估土壤中PFAS的污染状况以及研究其在土壤中的行为至关重要。
目前,针对PFAS的检测手段涵盖了电化学法[13]、酶联免疫吸附法[14]、气相色谱-质谱法[15]、液相色谱-串联质谱法等[16-17]。电化学技术在设备要求上较为简单,检测速度快,但选择性有限,难以同时对多种PFAS化合物进行测定;酶联免疫法操作过程复杂,特异性不足,可能导致假阳性结果;气相色谱-质谱法适用于分析挥发性较好的PFAS,但对于非挥发性或极性较强的化合物,需要进行较为繁琐的样品前处理;液相色谱-串联质谱法作为当前检测的主流技术,融合了液相色谱的高分离能力和质谱的高灵敏度与特异性,是分析复杂样品中PFAS的理想工具。
在国内外文献中,土壤的萃取方法有加压流体萃取、超声萃取、振荡萃取、微波萃取等[18-22]。振荡萃取虽然能达到理想的提取效果,但需要较长时间的振荡,且试剂消耗量也较大;超声萃取利用空化和粉碎作用加速溶剂渗透以提高提取效率,但强烈的超声波可能造成PFAS组分的部分损失;微波萃取则因其快速、低溶剂消耗、不破坏分析形态完整性以及回收率不受含水率影响等优点,能够获得较高的回收率和数据稳定性,成为一种高效的萃取方法。
全自动固相萃取法(ASPE)作为一种自动化样品前处理技术,因其操作简便、高效、稳定和重现性良好而受到青睐。李双双等[23]采用ASPE-超高效液相色谱-串联质谱法(ASPE-UPLC-MS/MS)对地表水中18种头孢菌素进行了测定,检出限为0.5~1.8 ng/L;姚志建等[24]则通过膜式固相萃取和液相色谱-串联质谱法分析了水样中17种全氟化合物,显著降低了检出限(0.2~0.3 ng/L),并获得了87%~95%的加标回收率;史丽等[25]开发了一种基于ASPE-UPLC-MS/MS的方法,用于测定污水中14种全氟化合物,验证了ASPE技术在去除复杂基体中干扰的应用潜力。然而,将该技术应用于土壤提取液样本中多种PFAS的快速富集和净化研究还相对不足。本研究采用微波萃取法,结合ASPE和UPLC-MS/MS技术,进行了一系列优化,包括微波萃取条件、ASPE条件及样品前处理流程,建立了一种准确、稳定且高效的方法,用于检测土壤中的PFAS。
1 实验部分 1.1 仪器、耗材与试剂 1.1.1 仪器与耗材仪器:SIL-40C X3型超高效液相色谱仪(日本SHIMAZU公司),配备了自动化采样单元、在线脱气装置、高压双泵系统和柱温箱;SCIEX Triple QuadTM 6500+型三重四极杆液质联用仪(美国AB公司),含2个独立运作的离子源(电喷雾电离源和大气压化学电离源);TANK 40型微波消解仪(上海新仪微波化学科技有限公司);E9000型自动固相萃取仪(广州盛康仪器有限公司),管路经过脱氟处理;电子天平(德国Sartorius公司)。
耗材:WAX固相萃取柱(6 cc/150 mg),HLB固相萃取柱(6 cc/200 mg),C18固相萃取柱(6 cc/500 mg),BEH C18色谱柱(1.7 μm,2.1 mm×50 mm),BEH C8色谱柱(1.7 μm,2.1 mm×50 mm),BEH Shiled RP18色谱柱(1.7 μm,2.1 mm×50 mm),BEH C18保护柱(1.7 μm,2.1 mm×5 mm),均购自美国Waters公司;LC-18固相萃取柱(6 mL/500 mg,德国Supelco公司)。
1.1.2 标准物质与试剂标准物质:22种PFAS标准物质混合溶液(2 μg/mL,纯度>95%,美国AccuStandard公司),包含全氟十四酸(PFTeDA)、全氟十三酸(PFTrDA)、全氟十二酸(PFDoDA)、全氟十一酸(PFUnDA)、全氟癸酸(PFDA)、全氟壬酸(PFNA)、全氟辛酸(PFOA)、全氟庚酸(PFHpA)、全氟己酸(PFHxA)、全氟癸烷磺酸(PFDS)、全氟壬烷磺酸(PFNS)、全氟辛烷磺酸(PFOS)、全氟庚烷磺酸(PFHpS)、全氟己烷磺酸(PFHxS)、全氟戊烷磺酸(PFPeS)、全氟丁烷磺酸(PFBS)、全氟辛基磺酰胺(PFOSA)、1,1,2,2-全氟癸烷磺酸(8 ∶ 2 FTS)、1,1,2,2-全氟辛烷磺酸(6 ∶ 2 FTS)、1,1,2,2-全氟己烷磺酸(4 ∶ 2 FTS)、N-乙基全氟辛烷磺酰氨基乙酸(N-EtFOSAA)、N-甲基全氟辛烷磺酰氨基乙酸(N-MeFOSAA)。17种PFAS标准物质混合溶液(2 μg/mL,纯度>90%,北京管理生物技术公司),包含PFDS、PFOS、PFHxS、PFBS、全氟丁酸(PFBA)、全氟戊酸(PFPeA)、PFHxA、PFHpA、PFOA、PFNA、PFDA、PFUnDA、PFDoDA、PFTrDA、PFTeDA、全氟十六酸(PFHxDA)、全氟十八酸(PFODA)。内标混合溶液(MPFAC-MXA)为7种质量标记13C的全氟烷基羧酸和2种质量标记18O和13C的全氟烷基磺酸盐,包含13C4全氟正丁酸(MPFBA)、13C2全氟正己酸(MPFHxA)、13C4全氟正辛酸(MPFOA)、13C5全氟正壬酸(MPFNA)、13C2全氟正癸酸(MPFDA)、13C2全氟正十一酸(MPFUndA)、13C2全氟正十二酸(MPFDoA)、全氟-1-[18O2]己烷磺酸钠(MPFHxS)、全氟-1-[13C4]辛烷磺酸钠(MPFOS),质量浓度均为2 μg/mL,化学纯度均>98%,同位素纯度均>99%,均购自加拿大Wellington Laboratories公司。
试剂:甲醇、乙腈(超纯液质联用级,美国Merck公司);甲酸、乙酸、乙酸铵(液质联用级,美国Merck公司);氨水(28.0%,优级纯,美国Sigma-Aldrich公司)。
1.2 标准溶液的制备内标使用液:采用95%甲醇将内标混合溶液稀释至200.0 ng/mL,并在4 ℃下密闭保存。
外标使用液:采用95%甲醇将22种和17种PFAS的混合标准溶液稀释,其中PFODA、PFHxDA、PFPeA、PFBA、N-EtFOSAA、N-MoFOSAA、8 ∶ 2 FTS、6 ∶ 2 FTS、4 ∶ 2 FTS、PFOSA、PFNS、PFHpS、PFPeS这13种PFAS的质量浓度为100.0 ng/mL,其余13种PFAS的质量浓度为200.0 ng/mL。
基质标准溶液:按下文1.3节所述方法处理空白样品,获得基质空白溶液。用基质空白溶液作为稀释液,对标准使用液进行逐级稀释,以此制备基质标准溶液系列,内标质量浓度为20.0 ng/mL。
1.3 样品制备取5.00 g土壤样本,将其转移至一个50 mL聚丙烯材质离心管中,加入15 mL 0.5%的氨水-甲醇溶液和10.0 μL内标使用液,涡旋混匀后进行微波提取。微波程序为:5 min加热到65 ℃保持25 min。在转速为2 800 r/min下离心10 min,分离提取液和固体颗粒,将上清液转移至另一个干净的聚丙烯离心管中,向该离心管加入100 mL水稀释,根据需要用5%的甲酸或3%的氨水调节pH值至6.5±0.5。
选择WAX柱作为富集净化柱,用全自动固相萃取仪对提取液进行净化处理。处理程序为:按序用5 mL 1%的氨水-甲醇溶液,5 mL 0.3 mol/L的甲酸溶液对WAX柱进行预处理;以5 mL/min的流速将稀释后的提取液通过WAX柱,然后依次用5 mL水、5 mL甲酸-甲醇溶液(V ∶ V=1 ∶ 1),以2 mL/min的流速淋洗固相萃取柱;真空抽气干燥WAX柱10 min;用5 mL 1%的氨水-甲醇溶液以2 mL/min的流速洗脱WAX柱,收集到的洗脱液在40 ℃下氮吹40 min。加入5 μL乙酸,用1%的氨水-甲醇溶液定容至1 mL,涡旋混匀后上机分析。
1.4 实验条件 1.4.1 质谱条件采用电喷雾负离子模式电离,在多重反应监测模式下进行质谱检测,气帘气为206.84 kPa,喷雾气为344.74 kPa,辅助加热气为379.21 kPa,离子源温度为300 ℃,离子化电压为-4 000 V。PFAS质谱分析参数见表 1(按化合物出峰顺序排列)。
| 表 1 PFAS质谱分析参数 |
选用BEH C18柱作为分析柱,配有BEH C18保护柱,流动相A为含2 mmol/L的乙酸铵和5%的乙腈水溶液,流动相B为乙腈;流速为0.40 mL/min;柱温选择40 ℃;进样量为2.00 μL。梯度洗脱程序:0~0.50 min,80%A;0.50~1.50 min,70%A;1.50~5.00 min,45%A;5.00~9.00 min,25%A;9.00~11.0 min,5%A;11.0~13.0 min,80%A。
1.5 质量控制为确保实验结果的准确性,在样品采集、处理和检测过程中避免使用含氟聚合物管线及其他可能引入PFAS的含氟材质的器皿,并在使用前对所用器皿用甲醇、纯水进行清洗。此外,每批样品至少包含1个全程序空白[26],以监控试剂或设备引起的背景污染。通过低质量浓度和中间质量浓度标准溶液的校准、溶剂空白分析和基体加标回收率检查,验证分析系统处于受控状态。
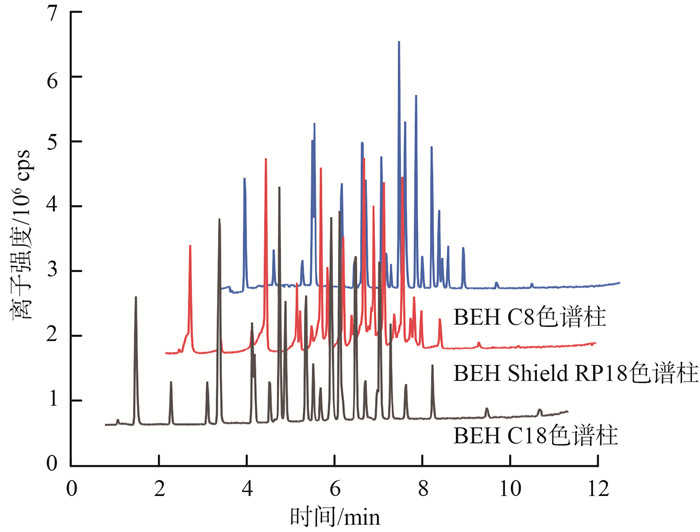
2 结果与讨论 2.1 色谱-质谱条件的确定 2.1.1 色谱条件的优化采用BEH C18、BEH C8、BEH Shiled RP18这3种色谱柱,对20.0 μg/L的标准溶液进行分析,分离效果见图 1。由图 1可见,采用BEH Shiled RP18柱,组分色谱峰出现变宽和变形,邻峰之间无法清晰地分离,分离效果不佳。对比固定相均为烷基官能团的反相色谱柱BEH C18和BEH C8,对分子量较大、疏水性较强的C12—C18化合物,BEH C18柱有更好的分离效果和稳定性。
|
图 1 3种色谱柱总离子流色谱图 |
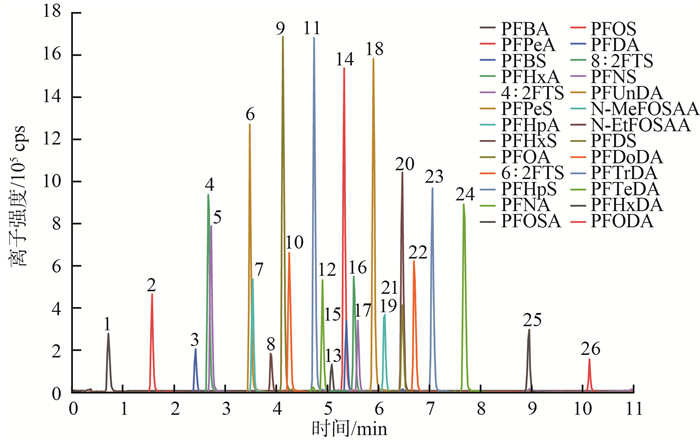
利用优化的色谱分析参数,成功实现了26种PFAS化合物的解析和测定,26个组分的色谱峰呈现锋利且均匀的对称形态,表现出良好的分离效果(图 2)。
|
图 2 26种PFAS标准溶液的多重反应监测色谱图 |
对三重四极杆串联质谱条件进行了优化。首先,将1.0 μg/mL标准溶液直接泵入质谱仪,在电喷雾负离子模式下进行全扫描,通过调节喷雾电压、鞘气、辅助气以及离子透镜电压等关键参数,获得目标化合物丰度较高的准分子离子峰。接着,选择这些准分子离子峰作为母离子进行二级质谱扫描,筛选出2个信号强度最高的特征碎片离子作为子离子,进一步优化子离子碰撞能量、去簇电压和裂解电压,最终得到了最佳的质谱参数(表 1)。
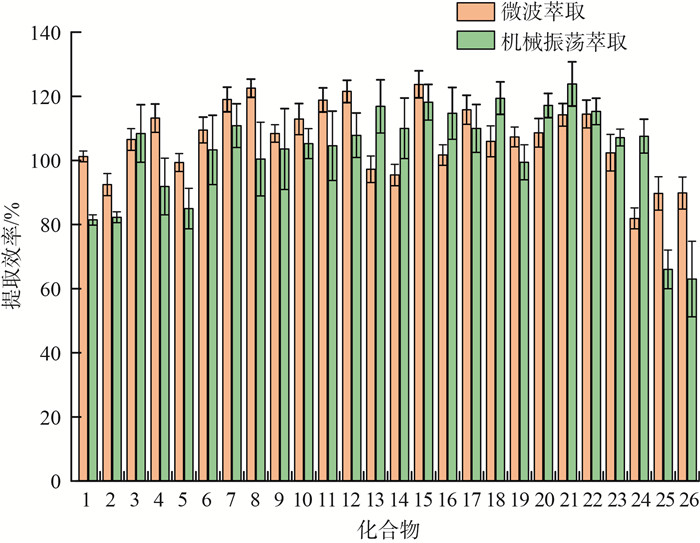
2.2 样品制备方式的确定 2.2.1 样品提取方式的优化本研究比较了常规机械振荡萃取和微波萃取对同一加标样品中26种PFAS的提取效率,结果见图 3(化合物序号同表 1)。由图 3可见,常规机械振荡萃取和微波萃取对土壤中短链和中链PFAS的萃取效率都比较好,但微波萃取对于易吸附在土壤颗粒上的长链PFAS的萃取效果明显优于常规机械振荡萃取。另外,常规机械振荡萃取耗时较长,一次需要耗费4~5 h,且溶剂消耗相对较大,而微波萃取处理一批样品耗时不超过1 h,高效快速、节能环保。因此,本研究采用微波萃取技术提取土壤中的PFAS。
|
图 3 不同萃取方式对目标化合物回收率的影响 |
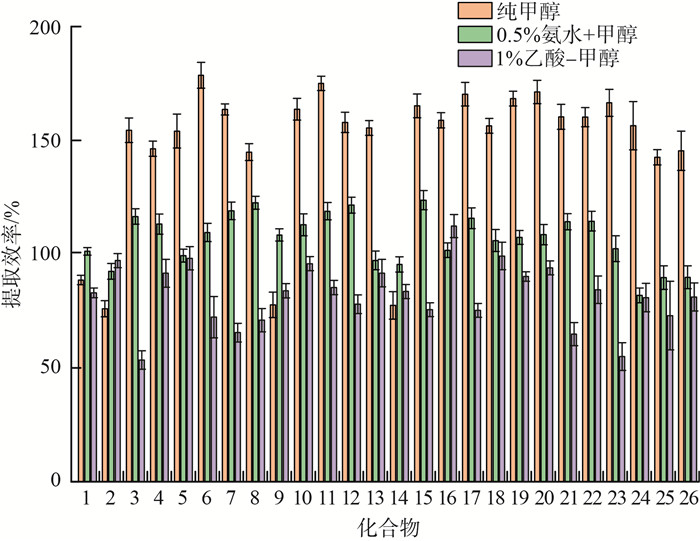
乙腈和甲醇是2种常用的有机提取溶剂,有文献表明,用乙腈做萃取剂时稳定性不如甲醇[27]。为了能够优先提取目标物质,而较少地萃取或不带出杂质,本研究比较了纯甲醇,含0.5%的氨水和含1%乙酸的甲醇溶液的提取效果,结果见图 4(化合物序号同表 1)。
|
图 4 不同提取剂对目标化合物回收率的影响 |
由图 4可见,加入少量氨水的甲醇溶液不仅能提高土壤中26种PFAS的提取效率,还能有效防止干扰物质被一起提取出来。这可能是由于26种PFAS中大部分以质子化或阴离子的形式存在,萃取剂呈弱碱性,使PFAS以游离形式存在,有利于增大在有机溶剂中的分配系数,从而增强其在甲醇中的溶解性,PFAS能够更有效地从土壤颗粒中释放出来,从而提高提取效率。因此,本研究选择含0.5%氨水的甲醇溶液作为土壤中PFAS的萃取剂。
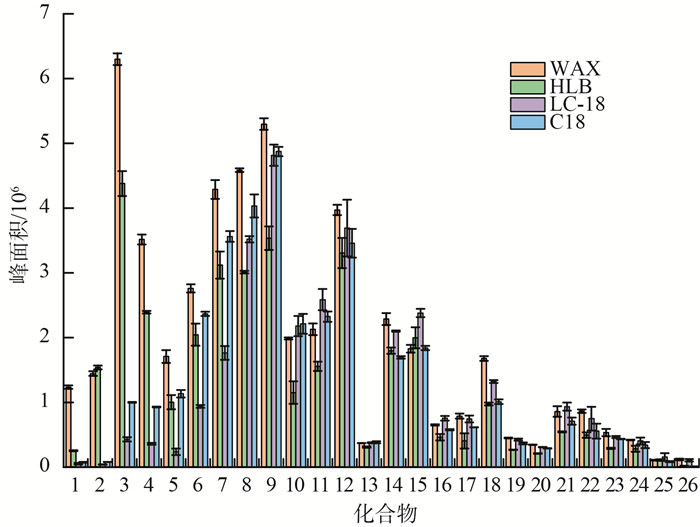
2.3 SPE条件的优化采用全自动固相萃取法对土壤样品的萃取液进行富集和净化,考虑到常用的固相萃取柱主要有HLB、WAX、LC-18、C18等类型[28-29]。HLB因其填料键合了亲水亲脂基团,广泛适用于各种类型有机物的富集净化分析;WAX柱基于混合型弱阴离子交换反相吸附剂的设计,适用于分离纯化酸性物质;LC-18多点键合,含有十八烷基,能够高效地提取非极性到中等极性的物质;C18因其具有疏水性和亲脂性,适用于分离和富集极性较弱的物质。综合考虑PFAS的物理、化学特性,本研究对比了上述4种SPE柱对26种PFAS的富集净化效果,结果见图 5(化合物序号同表 1)。
|
图 5 不同类型固相萃取住对目标化合物峰面积的影响 |
由图 5可见,HLB柱对C4—C9 PFAS的富集效率明显低于WAX柱,且对PFODA几乎未检出;LC-18和C18柱对C8—C16 PFAS的富集效率优于HLB柱,但仍低于WAX柱,且C18柱对PFODA也几乎未检出;WAX柱对26种PFAS的富集效率均优于HLB、LC-18和C18柱,表现出高富集效率和良好的净化效果,回收率也是4种SPE柱中最高的。基于上述结果,本研究选择WAX柱作为土壤样品PFAS提取液的富集净化柱。
2.4 方法学考察 2.4.1 基体效应土壤样品成分复杂,表现出显著的基体效应。通过对比分析土壤空白基体提取液中加入的外标使用液与以95%甲醇溶液为溶剂的相同质量浓度的混合标准溶液在ASPE-UPLC-MS/MS测定中的结果,评估了土壤样品的基体效应。基体效应计算公式见式(1)[30]。
| $ \mathrm{ME}=(A \mathrm{~s}-A \mathrm{x}) / A \mathrm{~s} \times 100 $ | (1) |
式中:ME——基体效应,%;As——使用95%甲醇配制的相同质量浓度的各种PFAS的峰面积;Ax——基体匹配混合标准溶液中各种PFAS的峰面积。当ME的值在0~±20%范围内,认为基体的影响可以忽略;在±20%~±50%范围内,表示存在中等程度的基体效应;>±50%时,则认为基体效应显著[31]。
研究结果显示,有16种PFAS展现了不同程度的基体效应,其中磺酸类PFAS的基体效应明显高于羧酸类PFAS,4 ∶ 2FTS(46.9%)、6 ∶ 2FTS(34.9%)、PFOSA(43.4%)、8 ∶ 2FTS(43.3%)、N-MeFOSAA(42.1%)、N-EtFOSAA(41.6%)的基体效应相对较高,处于中等程度,而其他PFAS的基体效应较小。因此,在分析实际土壤样品时,为了最大限度地减少基体效应的干扰,需要采用基质匹配标准曲线来进行PFAS的定量分析。
2.4.2 标准曲线、方法检出限和测定下限用无样本提取液作为基质,配制出一系列不同质量浓度的PFAS混合标准溶液,质量浓度分别为1.0(2.0),5.0(10.0),10.0(20.0),20.0(40.0),50.0(100)ng/mL(有的组分在1个混标里有,质量浓度是括号前的数字,有的组分在2个混标里有,质量浓度是括号里的数字),含内标为20 ng/mL,按照质量浓度从低到高的顺序进样。采用各组分的质量浓度作为独立变量,各组分和内标峰面积的比值作为因变量,进行线性回归分析。结果显示,26种PFAS在0.5(1.0)~50.0(100) μg/L的质量浓度范围内表现出良好的线性关系,相关系数(r)均>0.995。对加标量为1.0(2.0) μg/L的空白样品,按照样品分析的全流程进行n次重复实验,根据《环境监测分析方法标准制定技术导则》(HJ 168—2020)[31]附录A中的公式计算方法检出限,将4倍检出限定为测定下限,结果见表 2。由表 2可见,26种PFAS的检出限范围为0.02~0.13 μg/kg,测定下限为0.08~0.52 μg/kg。
| 表 2 26种PFAS的校准曲线、相关系数、方法检出限和测定下限 |
为了评估方法的准确度和精密度,本研究对土壤样品进行低、中、高3个质量分数水平的加标回收实验。向土壤样品中分别添加1.2节所述的外标使用液,使加标质量分数分别为1.0,5.0,20.0 μg/kg,按照1.3节所述方法进行样品处理,每个加标质量分数都进行3次平行实验,计算加标回收率和相对标准偏差(RSD),结果见表 3。
| 表 3 26种PFAS的准确度和精密度(n=3) |
由表 3可见,3个加标质量分数的回收率为63.5%~112.3%,RSD为0.4%~18.8%,表明本方法不仅具有较好的准确度,也具有较高的精密度,适用于实际土壤样品中26种PFAS的分析。
3 结语本研究通过精细的实验优化,建立了基于微波萃取、全自动固相萃取和超高效液相色谱-串联质谱(ASPE-UPLC-MS/MS)技术同时测定土壤中26种PFAS的分析方法。该方法使用0.5%氨水-甲醇溶液进行微波提取,WAX柱进行全自动SPE净化浓缩,简化了样品前处理过程。在优化的实验条件下,26种PFAS在特定的质量分数区间内表现出良好的线性响应,加标回收率为63.5%~112.3%,RSD均<20%,充分验证了本方法在准确性、灵敏度和重复性等方面的优势。因此,该方法对土壤样品中26种PFAS的精确测定具有显著适用性,为土壤监测领域典型及新型PFAS污染物的有效监控提供了有力支持。
| [1] |
BUCK R C, FRANKLIN J, BERGER U, et al. Perfluoroalkyl and polyfluoroalkyl substances in the environment: Terminology, classification, and origins[J]. Integrated Environmental Assessment Management, 2011, 7: 513-541. |
| [2] |
AHRENS L, BUNDSCHUH M. Fluorochemical use, distribution and release overview[R]. MN: 3M Company, 1999.
|
| [3] |
US EPA. Our current understanding of the human health and environmental risks of PFAS[R]. United States Environmental Protection Agency, 2022.
|
| [4] |
WANG Z, DEWITT J C, HIGGINS C P, et al. A never-ending story of per-and polyfluoroalkyl substances(PFASs)?[J]. Environmental Science & Technology, 2017, 51: 2508-2518. |
| [5] |
VESTERGREN R, HERZKE D, WANG T, et al. Are imported consumer products an important diffuse source of PFASs to the Norwegian environment?[J]. Environmental Pollution, 2015, 198: 223-230. |
| [6] |
BE CANOV'A J, MELYMUK L, VOJTA S, et al. Screening for perfluoroalkyl acids in consumer products, building materials and wastes[J]. Chemosphere, 2016, 164: 322-329. |
| [7] |
胡婷婷. 生态纺织品中三类毒物检测方法建立及其安全预警研究[D]. 长春: 吉林大学, 2017.
|
| [8] |
张悦清, 张爱国, 曹莉, 等. 长江流域全氟化合物污染态势与生态效应[J]. 环境监控与预警, 2020, 12(5): 58-67. |
| [9] |
WANG Z, BUSER A M, COUSINS I T, et al. A new OECD definition for per-and polyfluoroalkyl substances[J]. Environmental Science & Technology, 2021, 55: 15575-15578. |
| [10] |
FALANDYSZ J, JIM'ENEZ B, TANIYASU S. Per-and polyfluorinated substances: An environmental update[J]. Chemosphere, 2022, 291: 132876. DOI:10.1016/j.chemosphere.2021.132876 |
| [11] |
郭萌萌, 崔文杰, 刘晓玉, 等. 黄渤海区域水产品中全氟烷基物质的分布特征[J]. 中国环境科学, 2020, 40(8): 3424-3432. DOI:10.3969/j.issn.1000-6923.2020.08.021 |
| [12] |
刘浩然, 邢静怡, 任文杰. 中国土壤中全氟和多氟烷基物质的分布、迁移及管控研究进展[J]. 环境科学, 2024, 45(1): 376-385. |
| [13] |
陈诗艳, 仇雁翎, 朱志良, 等. 土壤中全氟和多氟烷基化合物的污染现状及环境行为[J]. 环境科学研究, 2021, 34(2): 468-478. |
| [14] |
张兴绘, 汤爱萍, 郭会琴, 等. QuEChERS-超高效液相色谱-串联质谱法测定昆虫体内35种全氟和多氟烷基化合物[J]. 环境化学, 2023, 42(4): 1137-1147. |
| [15] |
RYU H, LI B, DE GUISE S, et al. Per-and polyfluoroalkyl substances(PFAS) in the environment: A review of their sources, fate, and toxicological effects[J]. Journal of Hazardous Materials, 2021, 408: 124437. |
| [16] |
贺锦灿, 张诗韵, 苏榆媛, 等. 典型全氟有机酸类化合物的样品前处理与分析方法研究进展[J]. 色谱, 2020, 38(1): 86-94. |
| [17] |
蒋海宁. Teflon材料及不粘锅涂层中的微量全氟辛酸(PFOA)的GC-MS测定研究[J]. 复旦学报(自然科学版), 2007, 46(3): 291-296. DOI:10.3969/j.issn.0427-7104.2007.03.006 |
| [18] |
孙 琳, 张欢燕, 周亚康. 高效液相色谱串联质谱法测定某市污水处理厂进出水中的全氟化合物[J]. 环境监控与预警, 2020, 12(5): 87-92. |
| [19] |
谢琳娜, 张海婧, 侯沙沙, 等. 固相萃取-超高效液相色谱-串联质谱法分析土壤中15种全氟化合物[J]. 分析化学, 2019, 47(12): 1967-1972. |
| [20] |
SCHRODER H F. Determination of fluorinated surfactants and their metabolites in sewage sludge samples by liquid chromatography with mass spectrometry and tandem mass spectrometry after pressurised liquid extraction and separation on fluorine-modified reversed-phase sorbents[J]. Journal of Chromatography A, 2003, 1020(1): 131-151. |
| [21] |
HIGGINS C P, FIELD J A, CRIDDLE C S, et al. Quantitative determination of perfluorochemicals in sediments and domestic sludge[J]. Environmental Science & Technology, 2005, 39(11): 3946-3956. |
| [22] |
STOCK N L, FURDUI V I, MUIR D C G, et al. Perfluoroalkyl contaminants in the Canadian arctic: Evidence of atmospheric transport and local contamination[J]. Environmental Science & Technology, 2007, 41(10): 3529-3536. |
| [23] |
李双双, 何媛媛, 杨紫薇. 全自动固相萃取-超高效液相色谱串联质谱法测定地表水中18种头孢菌素[J]. 环境监控与预警, 2024, 16(1): 51-55. |
| [24] |
姚志建, 顾凯丽, 李涛, 等. 基于膜式固相萃取的水体全氟化合物检测方法研究[J]. 环境科技, 2024, 37(2): 40-45. |
| [25] |
史丽, 王兴, 杨艳, 等. 固相萃取-高效液相色谱-串联质谱检测污水中14种全氟化合物[J]. 化学研究与应用, 2024, 36(3): 647-654. |
| [26] |
刘承友, 刘金林, 郭婧, 等. 大伙房水库多介质中全氟化合物赋存特征、源解析及健康风险评估[J]. 环境监控与预警, 2022, 14(5): 133-142. |
| [27] |
申楠, 韩同竹, 盛璨璨, 等. 在线固相萃取净化-液相色谱-串联质谱法直接测定植物粗提物中的23种全氟化合物[J]. 分析化学, 2024, 52(2): 286-300. |
| [28] |
PAN Y Y, SHI Y L, CAI Y Q. Determination of perfluorinated compounds inhuman blood samples by high performance liquid chromatography-electrospray tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2008, 36(10): 1321-1326. |
| [29] |
YAMASHITA N, KANNAN K, TANIYASU S, et al. Analysis of perfluorinated acids at parts-per-quadrillion levels in seawater using liquid chromatography-tandem mass spectrometry[J]. Environmental Science & Technology, 2004, 38(21): 5522-5528. |
| [30] |
WANG Y N, CHEN J H, HE X P, et al. Study on rapid and non-destructive detection method for loquat fruit quality based on near-infrared spectroscopy technology[J]. Chinese Journal of Analytical Chemistry, 2021, 49(2): 282-291. |
| [31] |
生态环境部. 环境监测分析方法标准制定技术导则: HJ 168—2020[S]. 北京: 中国环境出版集团, 2020.
|
 2025, Vol. 17
2025, Vol. 17 