喹诺酮类抗生素(QNs),又称为吡酮酸或吡啶酸类,主要有氧氟沙星、左氧氟沙星和诺氟沙星等,属于广谱抗菌药,其特点是抗菌活性强、吸收好、少有交叉耐药,早期主要用于疾病医疗和畜牧业[1-3]。近年来,随着水产养殖业快速发展,养殖模式转变为规模化养殖,大量投饵和滥用抗生素等使养殖水环境污染加剧[4-5]。有研究表明,约52%的抗生素被用于畜牧业和水产养殖[6],其在养殖尾水中的残留会引发环境风险[7],特别是对人体健康的潜在威胁日益引起广泛关注[8]。
目前针对环境水体中抗生素,国家尚未发布统一的监测方法标准,水体中抗生素的研究分析主要采用液相色谱法,具体分为固相萃取-高效液相色谱-荧光检测法(SPE-HPLC-FD)、固相萃取-高效液相色谱-紫外检测法(SPE-HPLC-UV)和固相萃取-液相色谱-串联质谱法(SPE-LC-MS/MS)[9-11],其中SPE-LC-MS/MS以高选择性的质谱作为检测器,检测灵敏度高、选择性好、准确度高,可以同时测定多种抗生素类污染物[12-13]。近年来,超高效液相色谱-质谱法广泛应用于各种抗生素痕量测定,李双双等[14]基于超高效液相色谱-串联质谱法(UPLC-MS/MS)建立了地表水中18种头孢菌素的高灵敏分析方法,能有效识别和定量分析地表水中头孢菌素的痕量浓度。仲伶俐等[15]建立了固相萃取技术结合超高效液相色谱-串联质谱法测定地表水中16种大环内酯和林可酰胺类抗生素,该方法测得的线性关系好,加标回收率高,精密度和准确度均可满足地表水中痕量残留的检测要求。
本研究聚焦于16种喹诺酮类抗生素,采用固相萃取与超高效液相色谱联合三重四极杆质谱,构建了一套针对养殖尾水环境中喹诺酮类抗生素的分析体系。选择江苏盐城3家典型的养殖区水产养殖尾水进行实样检测,以期为渔用喹诺酮类抗生素监管提供数据支撑。
1 实验部分 1.1 仪器耗材与试剂 1.1.1 仪器耗材仪器与耗材见表 1。
| 表 1 仪器与耗材 |
实验试剂见表 2。
| 表 2 实验试剂 |
标准溶液配制:用甲醇将100 mg/L的16种喹诺酮类混标溶液和诺氟沙星-D5内标溶液稀释100倍,配制成质量浓度为1 000 μg/L的混标和内标使用液,将2种使用液合并。用体积分数为0.5%的甲酸-5 mmol/L甲酸铵溶液与甲醇以90 ∶ 10的体积比混合,用其将使用液稀释至所需浓度。
1.2 样品采集与处理 1.2.1 样品采集分别对3家典型的养殖区水产养殖尾水每月进行1次采样监测,采样时间为2023年10月—2024年3月。
使用1 000 mL磨口或具聚四氟乙烯内衬垫瓶盖的棕色玻璃瓶采集水样,水样经盐酸调节pH值≤2后在4 ℃下冷藏、密封、避光保存,7 d内完成萃取后,萃取液于-15 ℃下冷冻、密封、避光保存,并在20 d内完成分析。
1.2.2 样品处理依次用6 mL甲醇、6 mL纯水和6 mL盐酸溶液将固相萃取柱完全浸泡进行活化。水样经0.45 μm混合纤维素(水系)微孔滤膜过滤后取1 000 mL,加入1 g乙二胺四乙酸二钠,以10 mL/min(约3~4滴/s)的流速通过固相萃取柱,上样完毕后用6 mL甲醇溶液(V甲醇 ∶ V水=1 ∶ 19)淋洗固相萃取柱,氮气吹干,再用10 mL体积分数为0.1%的甲酸-甲醇溶液以1 mL/min的流速洗脱,用洁净试管收集洗脱液。用浓缩装置把洗脱液浓缩至近干,加入内标使用液10.00 μL,用初始流动相定容至1 mL,用涡旋混匀器混匀后经0.22 μm滤膜过滤,置于样品瓶中,待测。
1.3 仪器条件 1.3.1 色谱条件采用BEH C18色谱柱(1.7 μm,2.1 mm×100 mm,美国Waters公司),流速为0.2 mL/min,进样量为10 μL,流动相A为0.5%甲酸-5 mmol/L甲酸铵溶液,流动相B为甲醇。色谱洗脱程序见表 3。
| 表 3 色谱洗脱程序 |
采用电喷雾离子源(ESI),并设置正离子检测模式(ESI+)进行扫描。数据采集采用了高度选择性的多反应监测模式(MRM)。此外,离子源电压为5 500 V,源温度为550 ℃,气帘气CUR压力为1.72×105 Pa,雾化气GS1压力为3.45×105 Pa,辅助气GS2压力为3.45×105 Pa,碰撞气CAD压力为4.14×104 Pa。优化后16种喹诺酮类抗生素的质谱参数见表 4。
| 表 4 优化后16种喹诺酮类抗生素的质谱参数① |
实验室质控通过校准曲线、实验室空白、平行样和基体加标来控制。标准曲线的相关系数应≥0.995,或相对响应因子的相对标准偏差(RSD)≤20%,且每20个样品或每批次样品(<20个)应测定1个标准曲线中间浓度点的标准溶液,其测定结果与该点浓度的相对误差应在±20%以内。实验室空白测定结果应低于方法检出限,平行样的相对偏差应在±25%以内,基体加标回收率应在40%~150%之间。
按照质谱参考条件(表 4)中确定的母离子与子离子进行监测,目标化合物保留时间的相对偏差的绝对值应<2.5%,且待测样品中各目标化合物定性离子相对丰度(Ksam)测定结果的偏差应保持在规定的最大容许范围内[16]。定性确证时离子相对丰度的最大允许偏差见表 5。
| 表 5 定性确证时离子相对丰度的最大允许偏差① |
通过前期查阅资料文献,重点考察了HLB柱[17-18],HLB填料主要是由亲脂性二乙烯苯和亲水性N-乙烯基吡咯烷酮单体组成的一种大孔共聚物,可以通过不同比例组合达到亲水与疏水的目的,从而萃取出不同极性的化合物。用HLB柱对16种喹诺酮类化合物进行空白水样加标回收实验,具体实验操作为:量取1 000 mL纯水,准确加入1 000 μg/L的16种喹诺酮类标准溶液使用液10 μL,按照1.2.2节进行样品处理,与绘制校准曲线相同的仪器分析条件进行测定,测得回收率在70%~120%之间,符合实验要求,因此选择HLB固相萃取柱。
2.1.1.2 洗脱溶剂的选择固相萃取柱的活化:分别用甲醇和纯水活化以及用甲醇、纯水和盐酸活化。结果显示,在酸性条件下,活化过的小柱洗脱效率要高于只用甲醇和纯水活化的小柱。
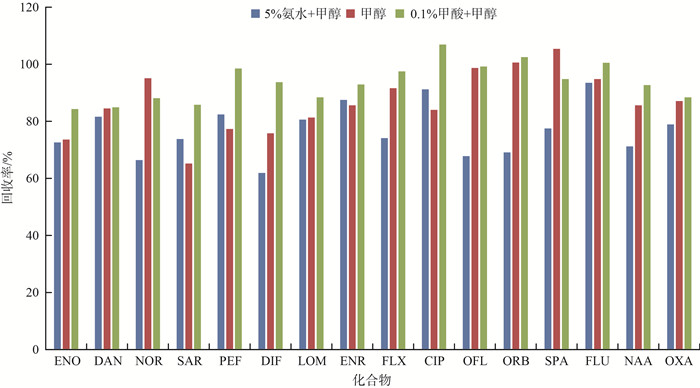
为了确保目标化合物能够被充分有效地从样品中分离出来,本研究进行比对实验来选出最优的洗脱条件。分别用纯甲醇、含有0.1%甲酸的甲醇溶液,以及添加了5%氨水的甲醇溶液对空白样品进行高、中、低质量浓度的加标回收实验,评估3种条件下的洗脱效率,结果见图 1。由图 1可见,0.1%甲酸+甲醇对各物质的洗脱效率最好,回收率可达80.5%~106.9%,而5%氨水+甲醇的回收率为61.9%~93.5%,甲醇的回收率为65.2%~105.4%,其效果均不如0.1%甲酸+甲醇。
|
图 1 3种洗脱条件对16种喹诺酮类抗生素洗脱效率的影响 |
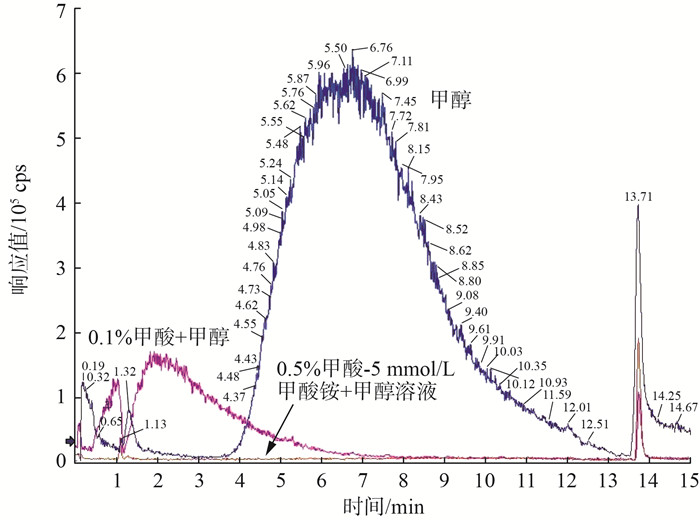
洗脱完成后,将洗脱液浓缩至近干,分别用甲醇,0.1%甲酸+甲醇以及等比例配制的0.5%甲酸-5 mmol/L甲酸铵+甲醇溶液(初始流动相)对洗脱液进行定容,定容体积为1 mL。3种不同定容溶液的空白总离子色谱(TIC)图见图 2。由图 2可见,用初始流动相定容的样品基线噪音较低且平稳,与标准使用液即校准曲线的配制保持一致。故选择0.5%甲酸-5 mmol/L甲酸铵+甲醇溶液作为定容溶液。
|
图 2 3种不同定容溶液的空白TIC图 |
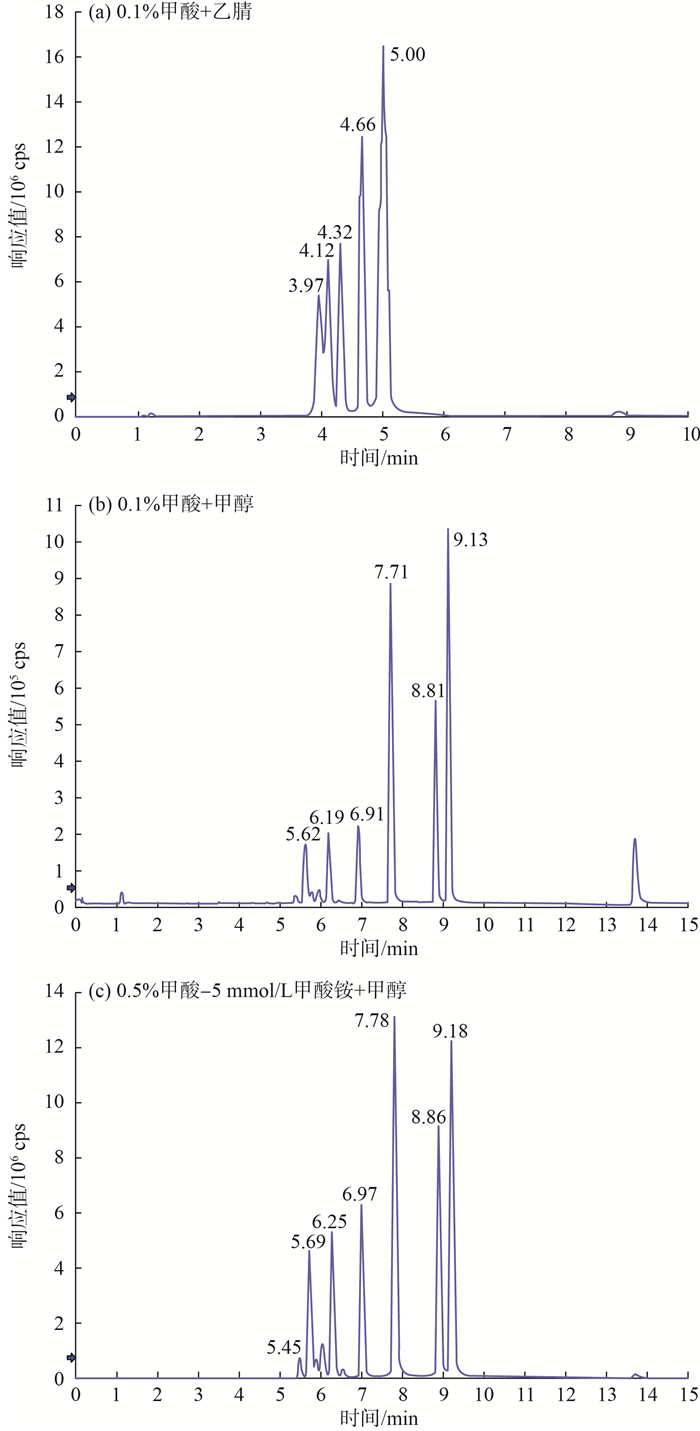
分别考察0.5%甲酸-5 mmol/L甲酸铵+甲醇、0.1%甲酸+甲醇和0.1%甲酸+乙腈3种流动相的分离效果。3种流动相的TIC图见图 3(a)—(c)。由图 3可见,流动相为0.1%甲酸+乙腈时,各组分物质出峰时间集中在4~8 min,各物质峰过于紧密,且部分物质分离效果不好,无法达到要求。流动相为0.1%甲酸+甲醇或0.5%甲酸-5 mmol/L甲酸铵+甲醇时,出峰时间集中在5~10 min,物质峰相对分散且峰线条平滑,峰型高尖,分离效果相对较好,其中流动相为0.5%甲酸-5 mmol/L甲酸铵+甲醇时,各组分物质的响应值相对更高,所以优先选择其作为流动相。
|
图 3 3种流动相的TIC图 |
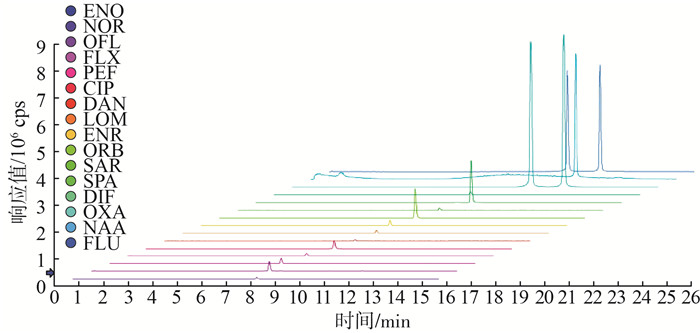
喹诺酮类抗生素基本都是在有机相增大的过程中洗脱出来的,但是有机相初始比例设置和增加速度的快慢都会影响分离效果。有机相增加速度过快会影响样品基线的稳定,增加速度过慢又会引起物质粘连、分离不开,而且梯度时间过长会增加批次样品的完成时间,使快速出具实验数据的效率降低。因此,经过反复实验调整,令有机相在1~12 min由10%增加到98%,此过程中,16种喹诺酮类抗生素在15 min内全部被分离,实验时长适中,优化后16种喹诺酮类抗生素的提取离子图见图 4。
|
图 4 优化后16种喹诺酮类抗生素的提取离子图 |
以目标化合物质量浓度为横坐标,以与其对应的峰面积(或峰高)与内标物峰面积(或峰高)的比值和内标物质量浓度的乘积为纵坐标,通过最小二乘法建立相关标准曲线,标准系列质量浓度梯度依次选择0,0.02,0.05,0.10,0.50,1.00,2.00,5.00,10.0,20.0,50.0,100 μg/L,内标质量浓度选择10.0 μg/L。根据响应不同,选择质量浓度范围不同。16种喹诺酮类抗生素的线性关系见表 6。由表 6可见,在检测灵敏度方面,OXA、NAA和FLU这3种化合物展现出最高的响应值,其线性范围下限可达0.02 μg/L;而SPA与ORB的响应值稍低,但依然能在0.05 μg/L的低质量浓度水平保持良好的线性关系;相比之下,NOR与DAN的响应值最低,线性范围下限为0.1 μg/L。其余化合物的响应表现各异,线性范围下限覆盖了0.02 ~0.1 μg/L的区间。16种喹诺酮类抗生素均展现出较好的线性关联性,相关系数分布在0.998 4~0.999 8的高水平范围内。
| 表 6 16种喹诺酮类抗生素的线性关系、方法检出限及测定下限 |
方法检出限的测定:由于仪器对不同物质的最低响应不一样,通过向1 L实验室空白水样中加入10 μg/L喹诺酮类抗生素标准溶液20和50 μL,使水样质量浓度为0.2和0.5 ng/L,分别重复测定7次。再根据公式(1)计算方法检出限,测定下限为4倍检出限。
| $ \mathrm{MDL}=t_{(n-1, 0.99)} \times S $ | (1) |
式中:MDL——方法检出限;t(n-1,0.99)——自由度为n-1,置信度为99%时的t分布,当n=7时,t(n-1,0.99)=3.143;S——n次平行测定的标准偏差。
由表 6可见,16种喹诺酮类抗生素的方法检出限为0.03~0.18 ng/L,测定下限为0.14~0.72 ng/L。16种喹诺酮类抗生素的检出限均低于以往研究水平[19],比起地方标准《水质喹诺酮类抗生素的测定液相色谱-串联质谱法》(DB 50/T 1366—2023)的检出限(2 ng/L)更是显著降低,特别是ORB、SPA、OXA的检出限均<0.05 ng/L。
2.3 准确度与精密度采集水产养殖池休渔期的排放尾水,选择合适的加标量,根据1.2节的预处理步骤,分别用水样配制0.2,2和20 ng/L的喹诺酮类抗生素标准溶液,每个质量浓度重复测定7次,以评估在低、中、高3种不同质量浓度水平下,实际水样中喹诺酮类抗生素的准确度与精密度,结果见表 7。由表 7可见,当加标量为0.2 ng/L时,16种喹诺酮类抗生素的回收率为64.9%~86.4%,相对标准偏差(RSD)为5.4%~14.6%;加标量为2.00 ng/L时,回收率为85.5%~107.7%,RSD为6.0%~13.0%;加标量为20 ng/L时,回收率为77.1%~94.0%,RSD为9.5%~14.5%。因此,该方法具有较好的准确度与精密度,不仅确保了定性、定量分析的可靠性,同时也展现了良好的稳定性,水样在预处理、固相萃取和仪器分析等全过程中所优化适配的条件参数能够达到对16种喹诺酮类抗生素进行全面有效检测的要求。
| 表 7 16种喹诺酮类抗生素的准确度和精密度(n=7) |
2023年10月—2024年3月,每月采集3家典型的养殖区水产养殖尾水,按照本研究确定的方法,对水样中16种喹诺酮类抗生素进行定量分析。其中,10—11月为养殖期,12月清塘,1—3月为休渔期。通过监测发现,养殖期因为药物投放,各水样中16种喹诺酮类抗生素大部分均有检出,质量浓度为0~432 ng/L,其中均有检出且质量浓度较高的物质依次是NOR(50.1 ~ 432 ng/L)、ENO(18.2 ~ 113 ng/L)和CIP(4.64 ~39.3 ng/L)。绝大部分水样中有检出的物质是SAR和DAN,质量浓度分别为0~ 74.7和0 ~58.9 ng/L;均未检出的物质是LOM、ORB和SPA。清塘期间各水样中喹诺酮类抗生素绝大部分均有检出,质量浓度为0~448 ng/L。休渔期间,各水样中喹诺酮类抗生素质量浓度大幅度降低,为0~29.3 ng/L。3月份,3家养殖尾水水样中的FLX质量浓度分别为0.39,0和1.73 ng/L,NOR质量浓度分别为0.46,0.06和0 ng/L,CIP质量浓度分别为1.18,2.71和0.43 ng/L,DIF质量浓度分别为0.37,0和0.63 ng/L。如果参照《DB 50/T 1366—2023》的检出限,以上物质均未检出,但是按照本研究的检出限(0.03~0.18 ng/L),质量浓度<1 ng/L的CIP和其余15个质量浓度<2 ng/L的物质,均可定量分析。
3 结语本研究选取了16种喹诺酮类抗生素作为研究对象,运用了固相萃取-超高效液相色谱-三重四极杆质谱,建立了一套适用于养殖尾水中喹诺酮类抗生素精准定量的检测方法。对固相萃取条件、液相色谱流动相组成与比例、梯度洗脱程序等各项参数进行调整与优化。对水产养殖尾水水样进行检测,结果发现其中含有不同质量浓度的喹诺酮类抗生素。以休渔期水产养殖排放尾水为基质进行加标回收实验,结果表明,加标回收率为64.9%~107.7%,RSD为5.4%~14.6%。该方法的准确度和精密度均较好,能够满足养殖尾水中多种喹诺酮类抗生素同时定量分析的要求。
| [1] |
陆茸, 杜尔登, 孙佳, 等. 太湖以西常州区域水体中典型PPCPs污染特征[J]. 环境监控与预警, 2021, 13(5): 133-137. |
| [2] |
秦永强, 任小玉, 鞠涵烨, 等. 海水中喹诺酮类抗生素液质联用测定前处理方法的优化[J]. 环境工程学报, 2022, 16(11): 3772-3783. |
| [3] |
张居舟, 李静. 在线固相萃取-同位素稀释/超高效液相色谱-串联质谱法测定蜂蜜中26种喹诺酮类化合物[J]. 分析测试学报, 2021, 40(10): 1417-1424. |
| [4] |
吕兑安, 程杰, 莫微, 等. 海水养殖污染与生态修复对策[J]. 海洋开发与管理, 2019, 36(11): 43-48. |
| [5] |
李贞金, 张洪昌, 胡双庆, 等. 2种氟喹诺酮类抗生素在水产养殖区沉积物上的吸附和解吸行为研究[J]. 生态毒理学报, 2023, 18(2): 434-448. |
| [6] |
陈昱如, 段艳平, 张智博, 等. 长江经济带水环境中抗生素人体健康风险评价[J]. 中国环境科学, 2023, 43(7): 3713-3729. |
| [7] |
王亚军, 陈甜婧. 氟喹诺酮类抗生素在水环境中的去除研究综评[J]. 环境监测管理与技术, 2021, 33(5): 1-5. |
| [8] |
陈晓燕, 周静峰, 施家威. 基质分散固相萃取-高效液相色谱-可变波长检测法测定新鲜牛奶中8种抗生素[J]. 食品安全质量检测学报, 2021, 12(12): 4812-4817. |
| [9] |
展海银, 周启星. 不同介质中四环素类抗生素的检出水平与污染扩散[J]. 生态学杂志, 2020, 39(12): 4206-4215. |
| [10] |
于辉, 赵萍. 快速溶剂萃取-高效液相色谱-紫外串联荧光检测法测定太平湖白鱼中4种氟喹诺酮类药物残留[J]. 中国食品卫生杂志, 2011, 23(4): 322-325. |
| [11] |
金晓峰, 焦仁刚, 赵贵, 等. 通过式固相萃取/超高效液相色谱-串联质谱法快速测定鸡蛋中的8种兽药残留[J]. 分析科学学报, 2020, 36(6): 906-911. |
| [12] |
廖杰, 李青松. 测定13种抗生素的固相萃取-高效液相色谱串联质谱法优化与应用[J]. 环境化学, 2022, 41(5): 1538-1547. |
| [13] |
吴建刚, 龙强, 肖文, 等. 环境水样中全氟磺酸类和全氟羧酸类化合物分析方法研究进展[J]. 环境化学, 2018, 37(8): 1851-1855, 1857-1859. |
| [14] |
李双双, 何媛媛, 杨紫薇. 全自动固相萃取-超高效液相色谱串联质谱法测定地表水中18种头孢菌素[J]. 环境监控与预警, 2024, 16(1): 51-55. |
| [15] |
仲伶俐, 郑幸果, 赵珊, 等. 超高效液相色谱-串联质谱法测定沼液中的林可霉素和大环内酯类抗生素[J]. 分析科学学报, 2021, 37(1): 57-62. |
| [16] |
重庆市市场管理局. 水质喹诺酮类抗生素的测定液相色谱-串联质谱法: DB 50/T 1366—2023[S]. 2023.
|
| [17] |
岳扬, 曲宝成, 刘鹰. 三氯蔗糖的环境污染及痕量检测技术研究进展[J]. 环境科学与技术, 2020, 43(7): 200-209. |
| [18] |
杨金泉, 贺小敏, 施敏芳, 等. 固相萃取-超高效液相色谱-串联质谱法同时测定地表水中9种性激素[J]. 中国环境监测, 2019, 35(3): 19-27. |
| [19] |
王锦, 叶开晓, 田艳, 等. 固相萃取-高效液相色谱-串联质谱法同时测定环境水样中22种抗生素[J]. 色谱, 2023, 41(3): 241-249. |
 2025, Vol. 17
2025, Vol. 17 

