有机氯农药(OCPs)是一类由人工合成的广谱杀虫剂,主要为以苯和环戊二烯为原料的六六六、滴滴涕、艾氏剂和狄氏剂等化合物,有机氯农药不易被代谢降解,进入生物体会积累,危害健康[1-2]。土壤基质复杂、成分多样,为准确检测其中的有机氯农药带来了各种难题,目前土壤有机氯农药的检测标准普遍采用《土壤和沉积物有机氯农药的测定气相色谱-质谱法》(HJ 835—2017)[3],标准中采用加压流体萃取法进行有机氯农药的提取,该方法需要使用昂贵的加压流体萃取仪,批量化程度也有局限。QuEChERS(快速-简便-廉价-高效-稳定-安全)前处理方法由Anastassiades等[4]科学家在固相萃取和基质固相分散基础上改进而来,核心是在萃取时加入合适的萃取盐进行有效分散和提取出目标组分,然后使用合适的净化材料净化提取液,有效保留目标组分并除去干扰,最初主要用于蔬菜或水果中农药残留的前处理[5-7],通过对提取和净化2个步骤的不断改进和优化,该方法已形成了一些行业标准[8-11]。因其操作简便、成本低、批量化强、绿色环保等优势引起广泛关注,也在多种土壤半挥发性有机化合物(SVOCs)的检测过程中得到应用[12-15],包括土壤中有机氯农药的检测[16-18],在研究人员所使用的条件及样品状态下,QuEChERS前处理法展现出了与传统方法相当的前处理能力,表现出了良好的精密度和正确度。
现通过土壤质控标准物质优化了前处理的提取时间和涡旋转速,比较了不同溶剂、萃取盐和净化剂对19种有机氯农药回收效果的影响,并采用对新鲜砂质土壤样品加标的方式进行方法的可行性验证,为方法的深入研究提供参考。
1 实验部分 1.1 仪器与试剂仪器:7890B-5977B型气相色谱-质谱仪(美国安捷伦公司);HP-5 MS毛细管色谱柱(30 m×0.25 mm×0.25 μm,美国安捷伦公司);HZY-B5000型电子天平(福州华志科学仪器公司);HD-2500型涡旋仪(济南欧莱博科学仪器有限公司);TD-4M型离心机(山东博科控股集团有限公司);EFAA-DC24型氮吹仪(上海安谱实验科技股份有限公司);UPH-I-100L型超纯水机(四川优润普科技有限公司)。
试剂:有机氯农药[α-六六六、六氯苯、β-六六六、γ-六六六、δ-六六六、艾氏剂、环氧化七氯、α-氯丹、α-硫丹、γ-氯丹、4,4′-滴滴伊(p,p′-DDE)、狄氏剂、β-硫丹、4,4′-滴滴滴(p,p′-DDD)、2,4′-滴滴涕(o,p′-DDT)、异狄氏剂醛、硫丹硫酸酯、异狄氏剂酮、灭蚁灵、七氯、异狄氏剂、4,4′-滴滴涕(p,p′-DDT)、甲氧滴滴涕]标准贮备溶液(100 mg/L,北京百灵威科技有限公司);土壤标准物质(200 μg/kg,北京百灵威科技有限公司,基质土壤为砂土);五氯硝基苯、菲-d10(内标,1 000 mg/L,北京百灵威科技有限公司);无水硫酸镁、氯化钠、无水硫酸钠(MgSO4、NaCl、Na2SO4,天津市科密欧化学试剂有限公司,分析纯,400 ℃马弗炉中焙烧2 h后使用);硅酸镁(MgSiO4,成都迈斯克医药科技有限公司,60~100目,400 ℃马弗炉中焙烧2 h后使用);QuEChERS萃取试剂(醋酸钠/无水硫酸镁、柠檬酸钠/无水硫酸镁,美国安捷伦公司)、QuEChERS净化试剂(PSA-MgSO4、C18-MgSO4,美国安捷伦公司);石英砂(60~100目,成都市科隆化学品有限公司,400 ℃马弗炉中焙烧2 h后使用);正己烷、丙酮、乙腈(色谱纯,成都迈斯克医药科技有限公司);超纯水(实验室自制,电阻率>18.25 MΩ·cm)。
1.2 样品采集实际土壤样品采集于某污染地块及周边,存放于棕色玻璃瓶,在0~4 ℃的冰箱中避光保存,土壤样品的水分含量根据《土壤 干物质和水分的测定重量法》(HJ 613—2011)[19]进行测定。
1.3 气相色谱-质谱仪测试条件色谱条件:载气为氦气(纯度为99.999%);恒流模式,流速为1.0 mL/min;进样口温度为250 ℃;进样模式为不分流进样;进样量为1 μL。柱温箱升温程序:初温80 ℃保持1 min,后以20 ℃/min速率升温至200 ℃保持1 min,再以5 ℃/min速率升温至250 ℃,然后以10 ℃/min速率升温至280 ℃保持1 min。
质谱条件:接口温度为280 ℃;离子源温度为230 ℃;电子轰击电离源(EI)能量为70 eV;样品数据采集模式为选择离子扫描模式(SIM)。
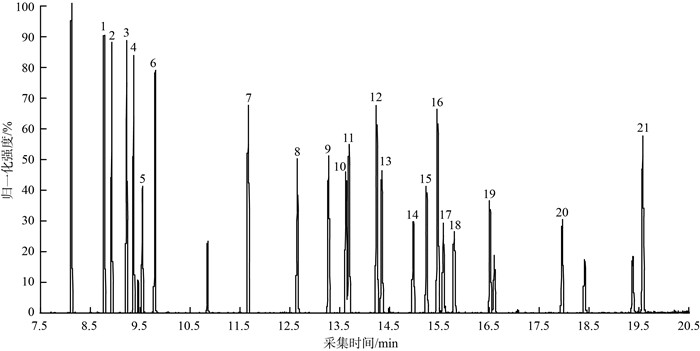
有机氯标准贮备溶液经逐级稀释配制成质量浓度为0.5,1.0,2.5,5.0,7.5,10 mg/L的标准系列溶液,按照上述仪器条件,全扫描模式(SCAN)采集得到总离子色谱图,通过对各组分的碎片离子进行分析,选择丰度最大的碎片离子作为对应组分的定量离子,选择合适的碎片离子作为定性离子,采用选择扫描组分的定量离子和定性离子进行样品测试。依次从低质量浓度到高质量浓度进样,以组分质量浓度为横坐标,组分与对应内标化合物的响应值的比值和内标化合物质量浓度的乘积为纵坐标,绘制校准工作曲线,19种有机氯农药在0.5~10 mg/L质量浓度范围内相关性良好,平均相对响应因子的相对标准偏差(RRF-RSD)为2.8%~12.8%。表 1为19种有机氯农药及内标的相关测试参数及结果,各组分的总离子流色谱图见图 1(图中数字对应表 1的编号)。
| 表 1 19种有机氯农药及内标的气相色谱-质谱测试条件及结果① |
|
图 1 19种有机氯农药及内标的总离子色谱图 |
称取2.00 g土壤样品(涡旋转速、提取时间、提取溶剂、萃取盐及净化剂试验采用土壤标准物质样品,方法回收率、精密度试验以及实际样品检测采用实际采集的新鲜土壤)于25 mL塑料离心管中(加标试验向离心管中加入一定量的标准溶液于土壤底部),加入2.0 mL超纯水涡旋混匀,静置10 min,加入萃取盐,同时加入5 mL溶剂,迅速加盖后涡旋一定时间,涡旋结束后取下离心管于4 000 r/min转速下离心5 min,移取上清液2.5 mL于装有净化剂的15 mL离心管中,涡旋净化5 min后再静置10 min,将净化液进行过滤,用5 mL正己烷洗涤净化剂,合并溶液氮吹浓缩至约0.5 mL,转移至2.0 mL棕色进样小瓶,加入内标使用液,正己烷定容至1 mL上机测定。所有数据均为3次试验的平均值,并以干重(干物质的测定按照《HJ 613—2011》执行)计算最终结果。
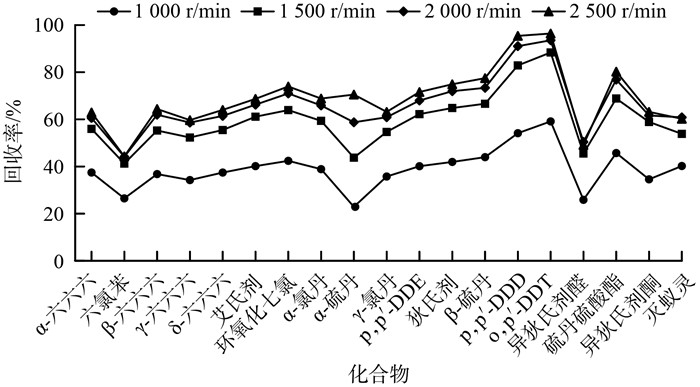
2 结果与讨论 2.1 涡旋转速试验涡旋时转速过低,无法有效分散土壤颗粒;转速过高,溶剂和土壤颗粒难以有效接触,设备长期处于高转速状态也会降低使用寿命。因此对1 000,1 500,2 000和2 500 r/min这4个涡旋转速进行探究。其他试验条件如下:提取时间为10 min,溶剂为正己烷/丙酮(V ∶ V=1 ∶ 1),萃取盐使用氯化钠/无水硫酸镁(0.5 g +0.5 g),无水硫酸钠/硅酸镁(0.5 g +0.5 g)作为净化剂,结果见图 2。
|
图 2 涡旋转速对19种有机氯农药回收率的影响 |
由图 2可见,涡旋转速对大多数组分回收率影响显著,随着转速的增大,19种有机氯农药的回收率均有所提高,转速由1 000 r/min增加到1 500 r/min时,组分回收率增长最为明显,1 500 r/min之后,组分回收率增加缓慢。在保证提取效率的同时兼顾仪器的性能,转速采用2 000 r/min。
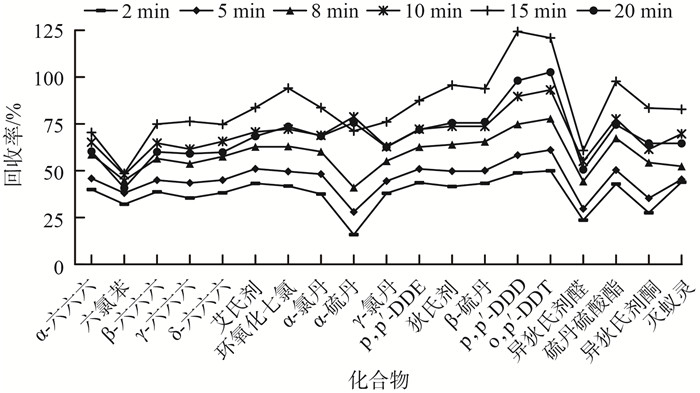
2.2 提取时间试验提取时间过短,无法充分提取出目标物;提取时间过长,会降低批量处理时的效率。因此考察了2,5,8,10,15和20 min这6个时长,其他试验条件同2.1节,结果见图 3。由图 3可见,提取时间为2~15 min,各组分的回收率均随提取时间的增加有明显的增长,受基质的影响,部分组分在15 min时的回收率已经在130%左右;而提取时间为20 min时,样品中大多数组分的回收率明显降低,其中部分组分降幅达到了20%。因此考虑在提高效率的同时降低基质的影响,提取时间选择10 min。
|
图 3 提取时间对19种有机氯农药回收率的影响 |
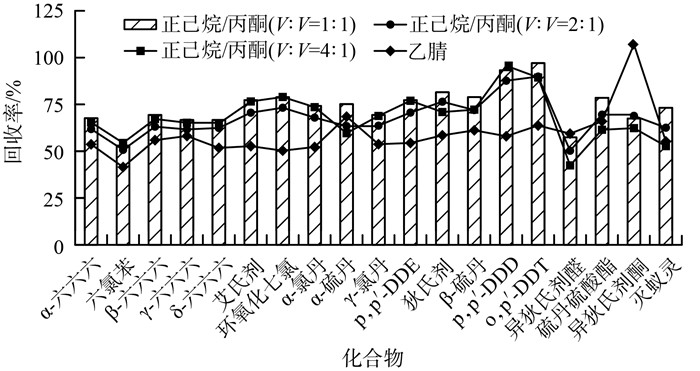
溶剂是有机氯组分被有效提取的关键条件,对正己烷和丙酮的体积比(1 ∶ 1,2 ∶ 1和4 ∶ 1)进行了比较并加入乙腈作为对比,其他试验条件同2.2节,结果见图 4。
|
图 4 溶剂对19种有机氯农药回收率的影响 |
由图 4可见,乙腈的提取效率总体比正己烷/丙酮体系低,而不同比例的正己烷/丙酮对大多数有机氯组分的回收率并未表现出较大的差异,与正己烷/丙酮(V ∶ V=1 ∶ 1)溶剂相比,大多数组分在正己烷/丙酮(V ∶ V=2 ∶ 1)溶剂中的回收率有所降低,而正己烷/丙酮(V ∶ V=4 ∶ 1)溶剂中也有部分组分的回收率降低,因此选择正己烷/丙酮(V ∶ V=1 ∶ 1)作为提取溶剂。
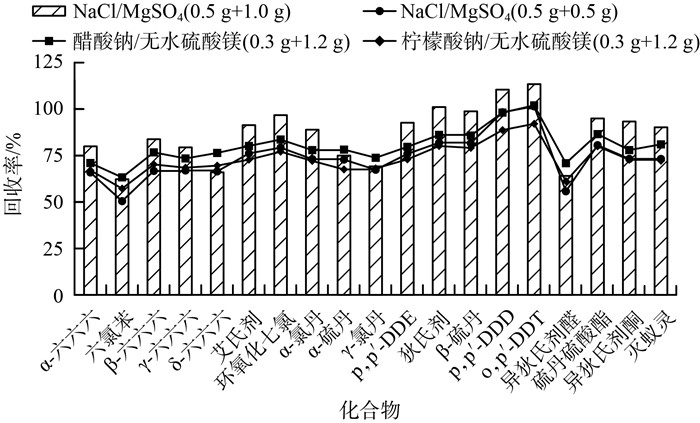
2.4 萃取盐试验萃取盐可以帮助分散土壤中的水分,使溶剂与土壤微粒充分接触,提取出吸附于土壤微粒中的有机氯组分,不同的萃取盐起到的分散效果不同,也就直接影响了对目标组分的提取效率。选择了NaCl/MgSO4(0.5 g+0.5 g)、NaCl/MgSO4(0.5 g+1.0 g)、醋酸钠/无水硫酸镁(0.3 g+1.2 g)、柠檬酸钠/无水硫酸镁(0.3 g+1.2 g)这4种萃取盐体系,其他试验条件如2.3节,结果见图 5。由图 5可见,相较于氯化钠/无水硫酸镁(0.5 g+0.5 g),使用醋酸钠/无水硫酸镁和柠檬酸钠/无水硫酸镁体系,大多数有机氯组分回收率有明显的降低,而使用NaCl/MgSO4在增加了MgSO4的含量后,19种有机氯组分的回收率均有明显的增长,因此萃取盐采用了回收率平稳的NaCl/MgSO4(0.5 g+1.0 g)的组合。
|
图 5 萃取盐对19种有机氯农药回收率的影响 |
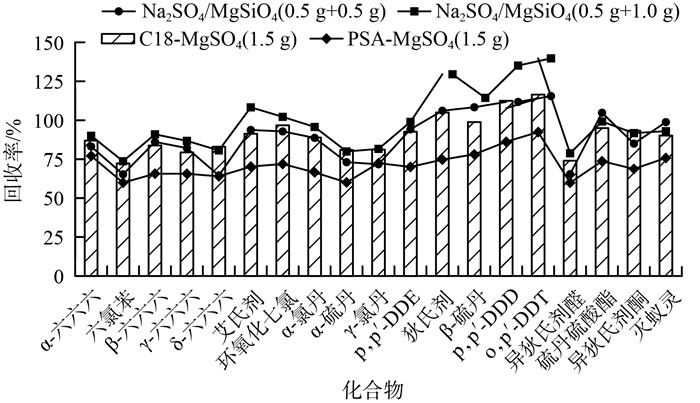
土壤中除了无机盐还有腐殖酸、脂肪等结构复杂的物质,未经有效净化而直接检测,则可能会出现基质增强或抑制的效应使结果偏离,试验考察了Na2SO4/MgSiO4(0.5 g+0.5 g)、Na2SO4/MgSiO4(0.5+1.0 g)、PSA-MgSO4(1.5 g)、C18-MgSO4(1.5 g)这4种净化剂,结果见图 6。由图 6可见,相较于Na2SO4/MgSiO4(0.5 g +0.5 g)作净化剂时,增加体系中的MgSiO4用量后,19种有机氯中大多数组分的回收率均有提高,但狄氏剂、o,p′-DDT的强基质效应并未有效控制,回收率>130%。净化剂PSA-MgSO4降低了一些组分的基质增强效应,但其中六氯苯、γ-六六六、δ-六六六和α-硫丹的回收率<70%。使用C18-MgSO4时,大部分组分的回收率有非常明显的增加,同时基质增强效应也得到抑制,19种有机氯组分的回收率保持在70%~120%之间。因此最终选择C18-MgSO4(1.5 g)作为净化剂。
|
图 6 净化剂对19种有机氯农药回收率的影响 |
优化后的前处理条件:涡旋转速为2 000 r/min,提取时间为10 min,正己烷/丙酮(V ∶ V=1 ∶ 1)为提取溶剂,NaCl/MgSO4(0.5 g+1 g)为萃取盐,使用C18-MgSO4进行净化,在该条件下采用新鲜砂质土壤(空白土壤经测试确认各组分均无检出)对方法的正确度和精密度进行了验证。在新鲜砂土中添加19种有机氯标准溶液,加标水平分别为0.5,2.0和5.0 mg/kg,按样品分析的全过程进行6次平行测试,计算各组分的加标回收率及相对标准偏差(RSD),同时按照样品分析的全过程重复7次空白加标试验(基体采用石英砂,加标量为4倍估计方法检出限值0.1 mg/kg),计算7次平行测定结果的标准偏差(S),按方法检出限(MDL)=t(3.143,n=7)×S计算,以4倍检出限作为测定下限,质量指标数据结果见表 2。由表 2可见,19种有机氯农药的加标回收率为68.5%~127.0%,平行测试的RSD为4.5%~23.0%,各组分的检出限范围为0.02~0.08 mg/kg。
| 表 2 19种有机氯农药的方法验证结果(n=7) |
在某污染地块及周边采集15份砂质土壤样品,按照优化后的试验条件进行了19种有机氯农药的测定,其中8份样品检出了狄氏剂,质量分数为0.02~0.06 mg/kg,6份样品检出了o,p′-DDT,质量分数为0.08~0.12 mg/kg,4份样品检出了灭蚁灵,质量分数为0.06~0.09 mg/kg。
3 结语基于QuEChERS前处理法结合气相色谱-质谱法测定了砂质土壤中的19种有机氯农药,使用质控样品对前处理条件进行了优化。结果表明,在0.5,2.0及5.0 mg/kg 3个加标水平下,19种有机氯农药的平均回收率为68.5%~127.0%,平行试验结果的相对标准偏差为4.5%~23.0%。该方法具有较好的正确度和精密度,方法快速简便,耗材成本低,试剂用量少,适用于批量操作,能够满足砂质土壤中19种有机氯农药的检测需求。
| [1] |
蔡道基, 杨佩芝, 汪竞立, 等. 有机氯农药在环境-生态系中的归趋与危害[J]. 生态学杂志, 1983, 2(1): 12-17. |
| [2] |
TAIWO A M. A review of environmental and health effects of organochlorine pesticide residues in Africa[J]. Chemosphere, 2019, 220: 1126-1140. |
| [3] |
中华人民共和国环境保护部. 土壤和沉积物有机氯农药的测定气相色谱-质谱法: HJ 835—2017[S]. 北京: 中国环境科学出版社, 2017.
|
| [4] |
ANASTASSIADES M, LEHOTAY S J, STAJNBAHER D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and "dispersive solid-phase extraction" for the determination of pesticide residues in produce[J]. Journal of AOAC International, 2003, 86(2): 412-431. |
| [5] |
MUSARURWA H, CHIMUKA L, PAKADE V E, et al. Recent developments and applications of QuEChERS based techniques on food samples during pesticide analysis[J]. Journal of Food Composition and Analysis, 2019, 84: 103314. |
| [6] |
李俊超, 秦学磊, 吴圣江, 等. QuEChERS前处理方法在食品检测中的应用进展[J]. 食品研究与开发, 2021, 42(24): 206-212. |
| [7] |
古汶玉, 何咏怡, 何梦婷, 等. QuEChERS在粮油产品农药残留检测中的应用现状[J]. 粮食加工, 2022, 47(2): 94-97. |
| [8] |
European Committee Standardization. Foods of plant origin-Multimethod for the determination of pesticide residues using GC-and LC-based analysis following acetonitrile extraction/partitioning and clean-up by dispersive SPE-Modular QuEChERS-method: EN 15662[S]. Brussels: European Committee for Standardization, 2018.
|
| [9] |
AOAC Official. Pesticide Residues in Foods by Acetonitrile Extraction and Partitioning with Magnesium Sulfate, Gas Chromatography/Mass Spectrometry and Liquid Chromatography/Tandem Mass Spectrometry: First Action 2007[S]. Rockville, MD: AOAC International, 2007.
|
| [10] |
国家卫生健康委员会, 农业农村部, 国家市场监督管理总局. 食品安全国家标准植物源性食品中208种农药及其代谢物残留量的测定气相色谱-质谱联用法: GB 23200.113—2018[S]. 北京: 中国标准出版社, 2018.
|
| [11] |
国家卫生健康委员会, 农业农村部, 国家市场监督管理总局. 食品安全国家标准植物源性食品中331种农药及其代谢物残留量的测定液相色谱-质谱联用法: GB 23200.121—2021[S]. 北京: 中国标准出版社, 2021.
|
| [12] |
VERA J, CORREIA-SÁ L, PAÍGA P, et al. QuEChERS and soil analysis—an overview[J]. Sample Preparation, 2013, 1: 54-77. |
| [13] |
李林凌, 席乐, 喻子恒. QuEChERS技术在土壤半挥发性有机物检测中的应用进展[J]. 山东化工, 2023, 52(21): 103-105. |
| [14] |
贺泽英, 张艳伟, 王雯雯, 等. QuEChERS-气相色谱三重四极杆串联质谱法测定土壤中227种农药残留[J]. 环境化学, 2020, 39(7): 2022-2025. |
| [15] |
蔡霖, 席普宇, 谢晴, 等. QuEChERS方法联合HPLC-MS/MS和GC-MS测定土壤中110种农药残留[J]. 农业环境科学学报, 2017, 36(8): 1680-1688. |
| [16] |
徐宜宏, 黄莹滢, 裴程程, 等. QuEChERS-气相色谱质谱法同时测定土壤中多种常见多氯联苯及有机氯农药[J]. 农药, 2018, 57(5): 351-354. |
| [17] |
吴东峰, 何伟忠, 王成. MAE-QuEChERS-GC法测定土壤中4种有机氯农药[J]. 分析仪器, 2020(1): 39-43. |
| [18] |
蔡灏兢, 程雪刚, 陈广银. QuEChERS-气相色谱法快速测定土壤中8种有机氯农药[J]. 环境监控与预警, 2020, 12(1): 25-28, 51. |
| [19] |
中华人民共和国环境保护部. 土壤干物质和水分的测定重量法: HJ 613—2011[S]. 北京: 中国环境科学出版社, 2011.
|
 2025, Vol. 17
2025, Vol. 17 